丁酰辅酶 A:从代谢物到表观调控信号
1. 引言
乙酰辅酶A(acetyl-CoA)通过作为组蛋白乙酰化的底物,将细胞能量状态与基因表达直接联系起来,已成为代谢-表观遗传调控的经典范例。然而,随着技术的发展,研究人员在组蛋白赖氨酸残基上陆续发现了多种新型短链酰基化修饰,包括巴豆酰化(crotonylation, Kcr)、丁酰化(butyrylation, Kbu)、β-羟基丁酰化(β-hydroxybutyrylation, Kbhb)等。这些修饰的发现极大地丰富了组蛋白翻译后修饰的类型,也为深入理解表观遗传调控机制提供了新的视角。
接下来将从丁酰辅酶A的代谢来源与区室化分布入手,系统阐述组蛋白丁酰化的酶学调控机制及其生物学功能,为相关领域的深入研究提供参考。
2. 丁酰辅酶A的代谢来源与区室化
2.1 内源性合成途径
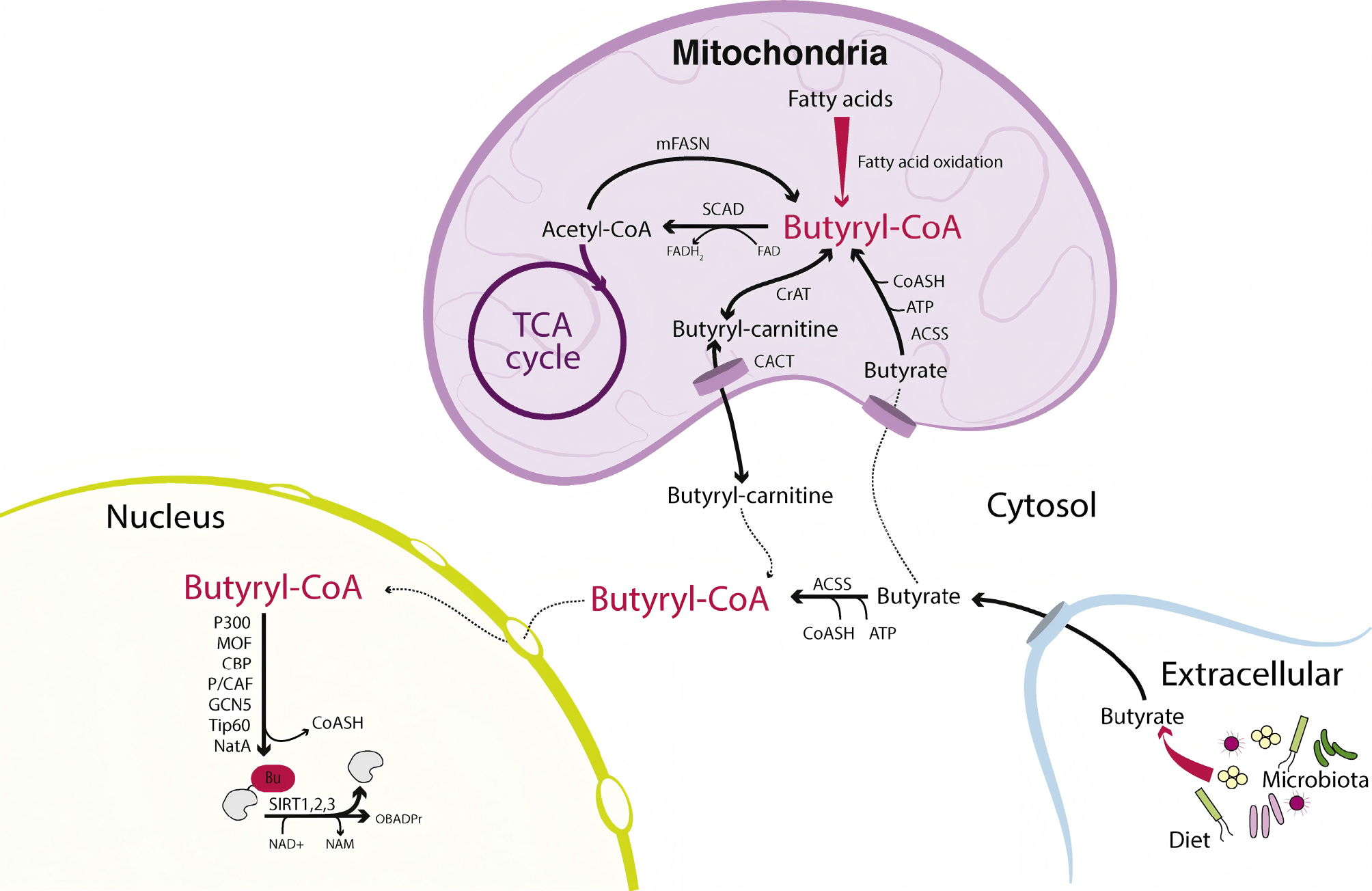
丁酰辅酶A在细胞内的产生主要源于脂肪酸代谢。在线粒体中,脂肪酸β-氧化每次循环缩短两个碳原子,其中丁酰辅酶A是短链脂肪酸(C4)氧化的中间产物。具体而言,丁酰辅酶A由巴豆酰辅酶A经烯酰辅酶A水合酶催化生成,随后可在短链酰基辅酶A脱氢酶(short-chain acyl-CoA dehydrogenase, SCAD)作用下进一步氧化为乙酰辅酶A。在SCAD缺陷的小鼠模型中,肝脏丁酰辅酶A水平可累积至与乙酰辅酶A相当甚至更高的水平,同时伴随全局赖氨酸丁酰化水平的显著增加,这一现象直接证实了内源性脂肪酸氧化与丁酰化修饰的密切关联。
此外,线粒体脂肪酸合成途径也能产生丁酰辅酶A,这一途径与脂酰化(lipoylation)过程偶联,为线粒体多种脱氢酶复合物(如丙酮酸脱氢酶、α-酮戊二酸脱氢酶)提供必需的辅因子。值得注意的是,线粒体内产生的丁酰辅酶A并不能直接跨越线粒体膜进入核质,其向核质的转运需要通过特定分子机制完成,这一过程也是丁酰化修饰精准调控的重要前提。
2.2 外源性来源:肠道菌群与丁酸的转化
丁酸是肠道菌群(如瘤胃球菌属、梭菌属、双歧杆菌属)发酵膳食纤维产生的主要短链脂肪酸之一,在人类大肠内容物中浓度可达24 mmol/kg,是肠道微生态与宿主代谢对话的关键媒介。丁酸可通过多种转运体(如单羧酸转运体1/4(MCT1/MCT4)、钠依赖型单羧酸转运体1(SMCT1))进入肠上皮细胞,随后在细胞质中经酰基辅酶A合成酶短链家族成员催化,与辅酶A结合转化为丁酰辅酶A。
值得注意的是,ACSS2的表达受固醇调节元件结合蛋白(sterol regulatory element-binding proteins, SREBP)转录因子调控,且该酶同时定位于细胞质和细胞核,这一亚细胞定位提示其可能在核内直接生成丁酰辅酶A,为核内组蛋白丁酰化修饰提供就地供应的酰基供体,避免丁酰辅酶A跨细胞器转运的时空限制。肠道来源的丁酸大部分被结肠上皮细胞作为能量底物代谢利用,仅有少量进入门静脉循环(浓度约14-64 μM),外周循环中浓度更低(1-12 μM)。因此,丁酰化修饰在与肠道直接接触的组织(如肠上皮)中尤为显著,在肝脏等门静脉回流器官中也有较高表达,这一定位特性决定了该修饰在肠道稳态和代谢调控中的特殊作用。
2.3 线粒体向核质的转运机制
丁酰辅酶A从线粒体向核质的转运是一个关键但尚未完全阐明的科学问题。首先,丁酰辅酶A可通过肉碱穿梭系统输出:线粒体肉碱乙酰转移酶(carnitine acetyltransferase, CrAT)可将丁酰辅酶A转化为丁酰肉碱,后者通过线粒体膜上的肉碱-酰基肉碱转运蛋白(carnitine-acylcarnitine translocase, CACT)转运至胞质,随后在胞质肉碱乙酰转移酶的催化下逆转转化为丁酰辅酶A,完成跨细胞器转运。
其次,线粒体产生的丁酸(通过硫酯酶水解丁酰辅酶A生成)可自由扩散至胞质,随后经ACSS2重新合成丁酰辅酶A,这一机制可绕过丁酰辅酶A直接跨膜的限制,实现代谢物的间接转运。此外,近年研究发现,部分代谢酶(如α-酮戊二酸脱氢酶复合物(OGDH复合物))可在核内定位,暗示核内可能存在独立的酰基辅酶A合成能力,无需依赖线粒体来源的丁酰辅酶A转运,但这一机制的具体分子细节仍需进一步验证。核内丁酰辅酶A的有效供应,为组蛋白丁酰化修饰的高效进行提供了物质基础,而这一修饰过程的精准调控则依赖于特定的酶学系统。
3. 组蛋白丁酰化的酶学调控
3.1 “写入器”:乙酰转移酶的混杂活性及竞争性调控
组蛋白丁酰化的“写入”过程主要由经典的组蛋白乙酰转移酶(HATs)催化,这类酶具有一定的混杂活性,可同时识别乙酰辅酶A和丁酰辅酶A作为酰基供体。研究表明,p300和环腺苷酸应答元件结合蛋白结合蛋白(CBP)是最有效的丁酰辅酶A利用酶,能够将丁酰基转移至核心组蛋白(H3、H4等)及非组蛋白(如p53、NF-κB)的赖氨酸残基上,调控其功能活性。体外酶活测定显示,p300/CBP对丁酰辅酶A的催化效率约为乙酰辅酶A的1/10至1/100,但仍显著高于其他HAT家族成员(如PCAF、GCN5)。
其他HATs如PCAF、GCN5、Tip60和MOF也表现出一定的丁酰转移酶活性,但效率较低且具有明显的位点特异性——例如,GCN5主要催化H3K14位点的丁酰化,而MOF则优先修饰H4K16位点。值得注意的是,丁酰辅酶A不仅是丁酰化的底物,还能竞争性抑制乙酰转移酶活性。丁酰辅酶A可结合至GCN5的活性中心,但其更长的酰基链会导致催化酪氨酸残基移位,破坏酶与乙酰辅酶A的结合位点,从而抑制酶活。
3.2 “擦除器”:去乙酰化酶的去丁酰化活性及丁酸的调控作用
组蛋白丁酰化的去除由经典的组蛋白去乙酰化酶(HDACs)和Sirtuin家族成员共同完成,两类酶的去丁酰化活性存在显著差异。生化测定显示,SIRT1-3具有较弱的去丁酰化活性,且仅对特定位点(如H4K5bu、H4K8bu)有识别能力;相比之下,I类HDACs(HDAC1-3)的去丁酰化效率更高,且对丁酰化底物的识别具有一定选择性——例如,HDAC2对H3K14bu的去除效率显著高于H3K9bu,这一选择性可能参与特定基因的精准调控。
在生理条件下,丁酸本身可作为HDAC抑制剂,通过非竞争性机制结合HDACs的活性中心,抑制其去乙酰化和去丁酰化活性,从而间接提高组蛋白乙酰化和丁酰化水平。这一双重作用机制使丁酸成为独特的表观遗传调节分子——既可转化为丁酰辅酶A直接作为修饰底物,又可抑制修饰去除酶活性,放大其调控效应,这也是肠道菌群通过丁酸调控宿主染色质状态的核心机制之一。
3.3 “阅读器”:丁酰化赖氨酸的特异性识别及功能差异
丁酰化修饰的生物学功能最终通过被特定“阅读器”蛋白识别而实现,与乙酰化修饰的阅读器存在显著差异。经典溴结构域(bromodomain)主要识别乙酰化赖氨酸,对丁酰化赖氨酸的亲和力普遍较低;然而,通过高通量筛选49个人源溴结构域发现,BRD9、CECR2的溴结构域以及TAF1的第二个溴结构域能够特异性结合丁酰化组蛋白肽段,其中BRD9对H3K14bu的结合亲和力可达乙酰化的3-5倍,提示这类溴结构域可能是丁酰化修饰的核心阅读器。
最具功能特征性的丁酰化阅读机制来自精子发生过程的研究。Goudarzi等(2023)发现,在小鼠精子发生后期,H4K5和H4K8位点的丁酰化水平显著升高,与乙酰化形成动态竞争;丁酰化修饰可延缓组蛋白的周转,并阻止转录调控因子溴域测试isomer(BRDT)的结合——而BRDT的乙酰化识别能力是精子发生后期基因表达调控的关键,这一发现首次揭示了丁酰化区别于乙酰化的独特功能:通过改变阅读器蛋白的招募模式,实现减数分裂后基因表达的精细调控。此外,近年研究发现,YEATS结构域家族蛋白也可能参与丁酰化赖氨酸的识别,但具体功能仍需进一步验证。
4. 丁酰化的生物学功能
4.1 动物系统中的功能
4.1.1 精子发生中的独特作用
丁酰化在精子发生后期的染色质重塑过程中具有核心调控功能。在小鼠精子发生过程中,减数分裂后生殖细胞会经历组蛋白逐步替换为鱼精蛋白(protamine)的过程,这一过程是染色质高度浓缩、精子成熟的必要条件;而H4K5/K8位点的丁酰化修饰可动态调控这一替换过程——丁酰化水平升高时,组蛋白替换速率减慢,确保染色质浓缩的正确时序,避免因替换过快导致的染色质损伤和精子活力下降。
CDYL(chromodomain Y-like转录共抑制因子)作为一种丁酰辅酶A水合酶,可通过催化丁酰辅酶A水解降低核内丁酰辅酶A水平,从而负向调控组蛋白丁酰化;其转基因小鼠模型表现为精子数量减少、活力下降及畸形率升高,最终导致生育能力降低,这一结果直接证实了丁酰化修饰在精子发生中的必要性。此外,近年研究发现,p300介导的H3K27bu修饰也参与精子发生过程中的基因表达调控,但具体机制仍需深入探讨。
4.1.2 代谢性疾病中的调控作用
近年来,丁酰化在代谢调控中的作用日益受到关注,尤其在肥胖相关高血压、糖尿病、非酒精性脂肪肝等代谢性疾病中,形成了“肠道菌群-丁酸-丁酰化”的独特调控轴。有研究结果表明:高脂饮食诱导的肥胖相关高血压大鼠出现肠道菌群紊乱,产丁酸菌(如瘤胃球菌属)丰度显著减少,导致血浆和粪便丁酸水平下降,进而引起肾脏组织中H3K9丁酰化修饰减少;而H3K9丁酰化的减少会导致保护性基因MAS1(MAS1原癌基因)表达降低,最终引发血压升高。
体外细胞实验表明,丁酸钠(丁酸的钠盐形式)可浓度依赖性地提升肾脏细胞H3K9丁酰化修饰及MAS1表达,逆转高脂饮食诱导的细胞损伤。这一研究首次将肠道菌群、代谢物、组蛋白修饰和疾病表型完整串联,为代谢性疾病的表观遗传调控提供了新范式。此外,在非酒精性脂肪肝模型中,丁酰化修饰可调控脂代谢相关基因(如PPARα、Cpt1a)的表达,减轻肝脏脂质积累,提示丁酰化可能成为代谢性疾病干预的新靶点。
4.1.3 癌症中的潜在角色
丁酸作为肠道菌群的代谢产物,在正常肠上皮细胞中可作为能量底物维持细胞稳态,但在结直肠癌细胞中,由于Warburg效应(癌细胞优先进行无氧糖酵解),丁酸无法被有效代谢而在细胞内积累;积累的丁酸可抑制HDAC活性,同时促进丁酰辅酶A生成,升高组蛋白丁酰化水平,进而诱导癌细胞凋亡、抑制细胞增殖。研究发现,H3K14bu在结直肠癌组织中表达显著低于正常肠黏膜组织,且其低表达与患者不良预后相关,提示丁酰化可能发挥抑癌作用。
在肝癌细胞中,丁酰辅酶A水平受高脂饮食调控,高脂饮食可通过抑制SCAD活性增加丁酰辅酶A积累,进而升高H3K9bu修饰水平,促进肝癌细胞增殖;而敲低ACSS2可减少核内丁酰辅酶A生成,降低H3K9bu修饰,抑制肝癌细胞迁移和侵袭。研究发现,丁酰化阅读器BRD9在肝癌组织中高表达,靶向抑制BRD9可降低丁酰化修饰的下游信号传导,抑制肝癌进展,为靶向丁酰化通路的抗癌治疗提供了新思路。目前,丁酰化在其他癌症(如胃癌、肺癌)中的功能仍处于探索阶段,其具体作用机制(抑癌或促癌)可能因癌症类型和微环境而异。
4.2 植物系统中的研究进展
相关研究初步揭示了丁酰化在植物逆境响应和发育调控中的重要作用。近期综述(Wei et al., 2025)系统总结了植物短链酰基化修饰的研究进展,其中对丁酰化的研究主要集中于水稻、拟南芥等植物。
在水稻中,组蛋白丁酰化(Kbu)被证实动态响应饥饿和淹水胁迫:淹水胁迫下,水稻幼苗中H3K14bu、H3K23bu和H4K5bu位点的修饰水平显著升高,且这一升高与胁迫响应基因SUBMERGENCE 1C(Sub1C)和CYTOCHROME P450(P450)的表达激活密切相关;染色质免疫沉淀实验证实,H3K14bu可富集于Sub1C基因的启动子区域,促进其转录表达,从而增强水稻的耐淹性。在饥饿胁迫(缺氮、缺碳)条件下,水稻叶片中H3K9bu修饰水平显著下降,伴随光合代谢相关基因的表达抑制,提示丁酰化可能通过调控代谢相关基因的表达,参与植物对营养胁迫的适应。
在拟南芥中,有研究首次鉴定出组蛋白丁酰化的“写入器”——拟南芥p300同源蛋白HAC1,该蛋白具有丁酰转移酶活性,可催化H3K14bu和H4K8bu修饰;HAC1突变体拟南芥表现为幼苗生长迟缓、耐旱性降低,且干旱胁迫响应基因DREB2A的表达显著下降,ChIP实验证实HAC1可通过介导DREB2A启动子区域的H3K14bu修饰,调控其基因表达,参与拟南芥的耐旱调控。
与动物类似,植物细胞中丁酰辅酶A可能主要来源于脂肪酸β-氧化途径,但植物作为自养生物,其丁酰辅酶A的代谢可能具有独特性——有研究提示,光合作用产物(如丙酮酸)可能通过线粒体代谢转化为丁酰辅酶A,但具体机制尚未明确。此外,植物中组蛋白丁酰化的“擦除器”和“阅读器”尚未被明确鉴定,核内丁酰辅酶A的生成与转运机制也缺乏深入研究。目前已鉴定出的植物组蛋白丁酰化位点包括H3K14、H3K23、H4K5、H4K8等,但这些修饰在植物生长发育(如开花调控、种子萌发)和其他逆境(如盐胁迫、低温胁迫)响应中的精确作用仍需深入探索。
4.3 代谢-表观遗传调控网络的整合视角
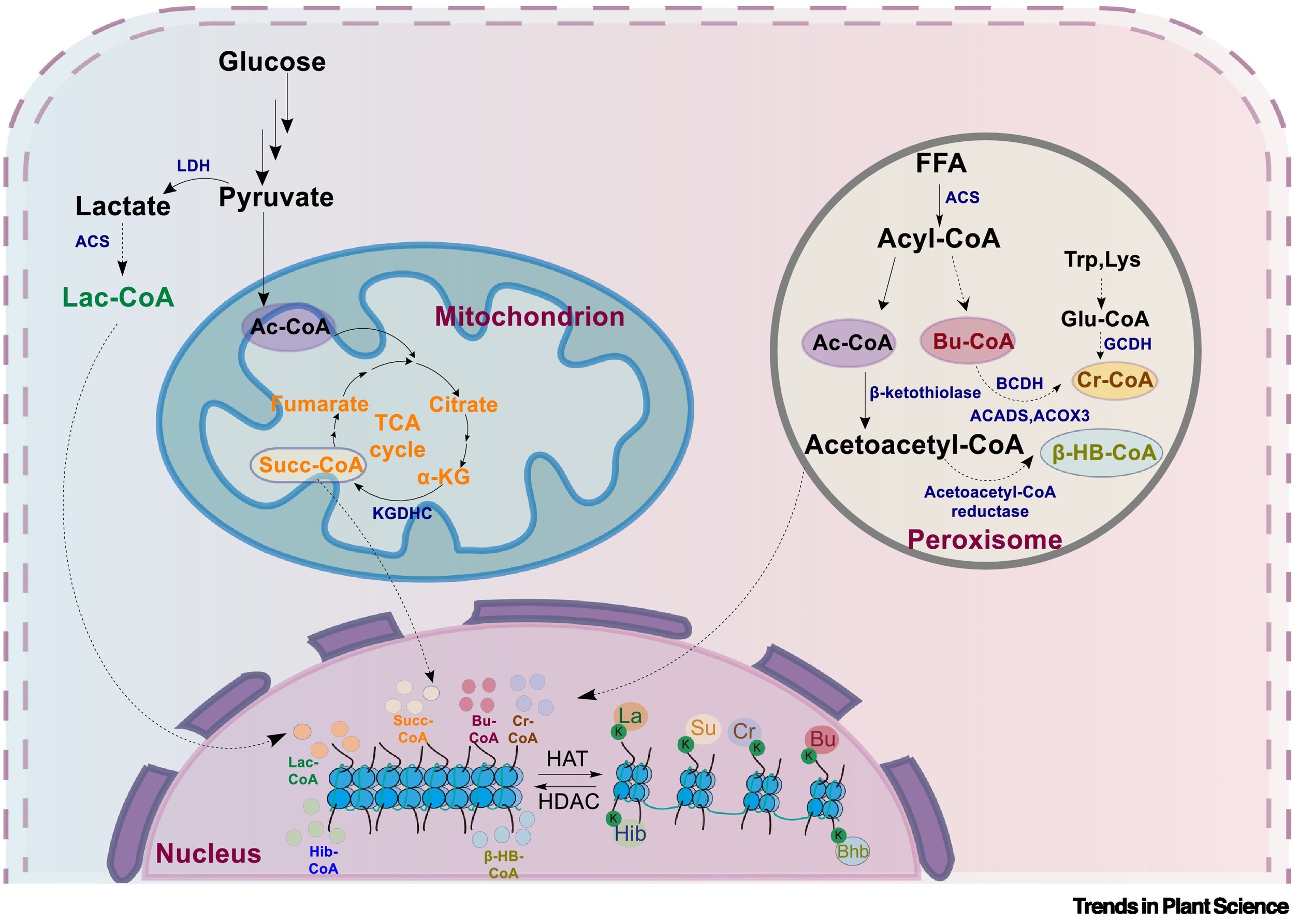
丁酰辅酶A的独特之处在于其处于代谢网络的核心节点,通过多种机制参与表观遗传调控,将细胞代谢状态与染色质功能、基因表达紧密关联,形成复杂的代谢-表观遗传调控,具体可分为以下三种机制:
机制一:直接作为酰基供体。丁酰辅酶A在p300/CBP等“写入器”酶的催化下,将丁酰基共价连接至组蛋白赖氨酸残基,改变染色质的压缩状态——丁酰基的疏水性强于乙酰基,可进一步松散染色质结构,促进转录因子结合,从而激活下游基因表达是丁酰化调控基因表达的核心途径。
机制二:竞争性调控乙酰化。丁酰辅酶A与乙酰辅酶A均可结合HATs的活性中心,二者形成竞争性结合关系——当细胞内丁酰辅酶A水平升高时,其与HATs的结合比例增加,抑制乙酰辅酶A的结合,从而降低组蛋白乙酰化水平。这种竞争性调控使细胞能够根据代谢状态(如脂肪酸氧化速率、肠道丁酸供应),动态调整乙酰化/丁酰化的平衡,实现基因表达的精细调控。
机制三:丁酸的双重作用。丁酸作为丁酰辅酶A的前体,具有双重表观遗传调控功能:一方面,丁酸可在ACSS2的催化下转化为丁酰辅酶A,为组蛋白丁酰化提供底物;另一方面,丁酸可作为HDACs抑制剂,非竞争性结合HDACs的活性中心,抑制其去乙酰化和去丁酰化活性,减少组蛋白修饰的去除,从而放大丁酰化和乙酰化的调控效应。这种双重作用使肠道菌群产生的丁酸能够高效调控宿主染色质状态,成为肠道微生态与宿主表观遗传对话的关键媒介。
这些机制相互协同、相互调控,共同构成一个复杂的代谢-表观遗传调控网络,使细胞能够根据内源性代谢状态(如脂肪酸氧化、能量供应)和外源性环境信号(如肠道菌群、营养供应),精细调节染色质修饰和基因表达,维持细胞稳态和机体正常生理功能。
结语
从经典的代谢中间产物到表观遗传调控分子,丁酰辅酶A的转变也揭示了“代谢-表观遗传-生理功能”的协同调控网络。对丁酰辅酶A和组蛋白丁酰化的深入研究,不仅将拓展我们对表观遗传调控原理的认知,完善代谢-表观遗传对话的理论体系,还将为代谢性疾病、生殖障碍、癌症等疾病的诊断和治疗,以及作物抗逆育种提供新的干预策略和分子靶点。




