巴豆酰辅酶A及其修饰:代谢枢纽与疾病调控的关键分子
1. 引言
巴豆酰辅酶A(crotonyl-CoA)是脂肪酸氧化、赖氨酸与色氨酸代谢过程中的重要中间代谢产物,同时也是蛋白质赖氨酸巴豆酰化修饰的直接供体。作为一种关键的代谢枢纽分子,巴豆酰辅酶A的水平变化直接影响细胞内赖氨酸巴豆酰化修饰的强度,从而将细胞代谢状态与蛋白质功能调控紧密联系起来。Kcr是一种进化上高度保守且广泛存在的蛋白质翻译后修饰,通过巴豆酰转移酶将巴豆酰基从巴豆酰辅酶A转移至目标蛋白的赖氨酸残基上。该修饰不仅存在于组蛋白,也广泛分布于非组蛋白,参与调控基因转录、染色质重塑、细胞周期进程及DNA损伤应答等多种生理过程。因此,巴豆酰辅酶A及其介导的巴豆酰化修饰在代谢调控与疾病发生中发挥着关键作用。
2. 巴豆酰辅酶A:来源、代谢与细胞区室化
2.1 化学结构与基本特性
巴豆酰辅酶A是丁酸发酵以及赖氨酸和色氨酸代谢的中间体。其结构特征在于含有一个α,β-不饱和双键(C=C),这一共轭体系赋予了巴豆酰基团独特的刚性平面构象。与乙酰辅酶A、丁酰辅酶A和琥珀酰辅酶A相比,巴豆酰辅酶A的不饱和结构使其在化学性质上更为稳定,对赖氨酸亲核试剂的反应活性较低,这可能解释了其非酶促修饰速率显著低于其他短链酰基辅酶A的现象。
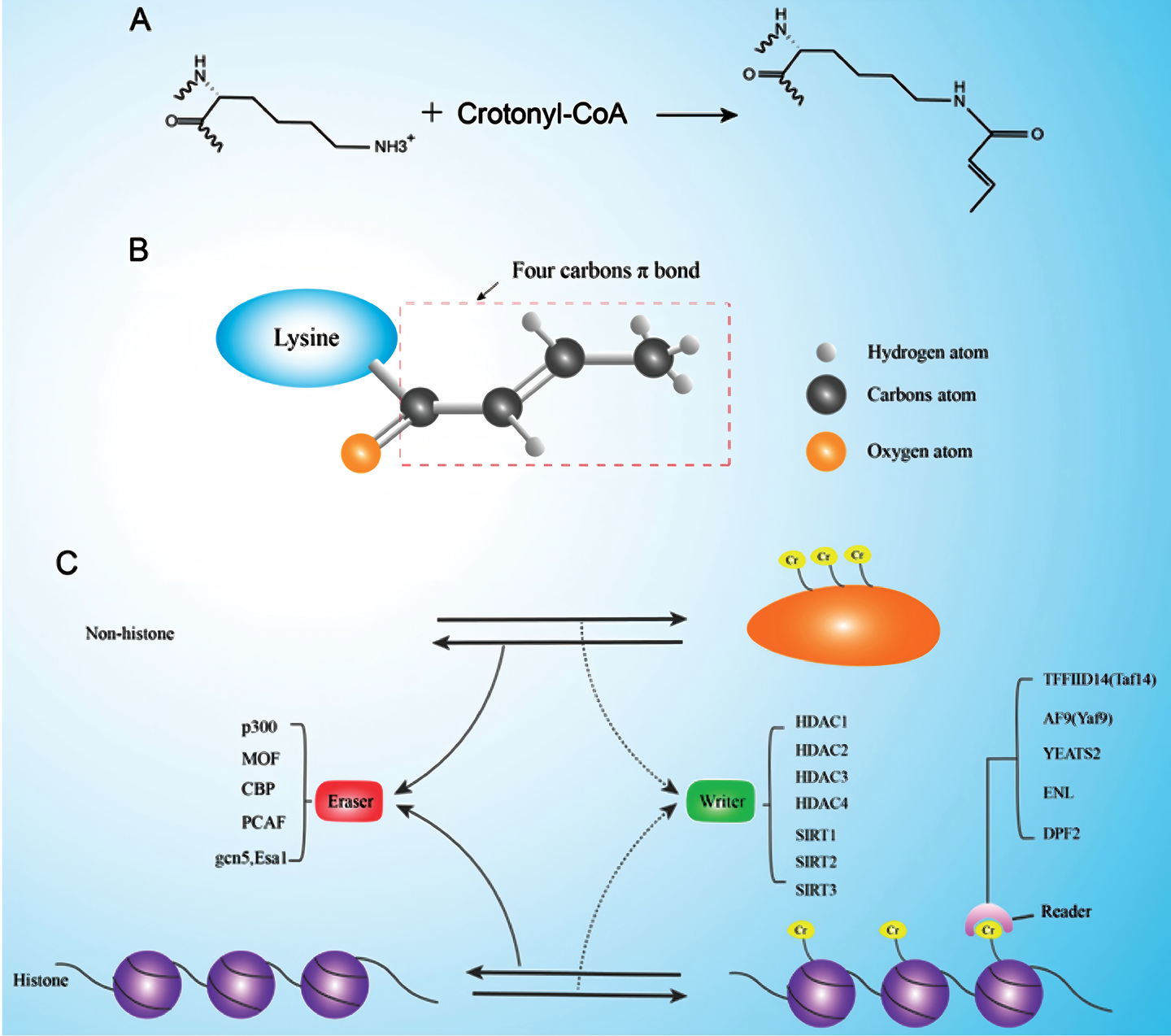
2.2 内源性合成途径
细胞内巴豆酰辅酶A主要通过以下三条代谢途径产生:
脂肪酸β-氧化途径:在线粒体中,短链脂肪酸(尤其是丁酸)通过β-氧化生成2,3-烯酰辅酶A中间产物,其中就包括巴豆酰辅酶A。酰基辅酶A脱氢酶短链(ACADS)可将丁酰辅酶A转化为巴豆酰辅酶A。此外,酰基辅酶A氧化酶(ACOX3)在胚胎干细胞内胚层分化过程中也被证实是巴豆酰辅酶A的重要来源。
氨基酸分解代谢途径:赖氨酸和色氨酸的分解代谢最终汇聚于α-酮己二酸,后者在α-酮戊二酸脱氢酶复合体(OGDHC)作用下转化为戊二酰辅酶A。戊二酰辅酶A脱氢酶(GCDH)催化戊二酰辅酶A氧化脱羧,通过酶结合的戊烯二酰辅酶A中间体生成巴豆酰辅酶A。此过程伴随FADH₂的产生,可直接参与电子传递链。
外源性巴豆酸的活化:巴豆酸(crotonate)作为短链脂肪酸,可通过酰基辅酶A合成酶短链家族成员2(ACSS2)催化生成巴豆酰辅酶A。ACSS2定位于胞浆和细胞核,其表达受SREBP转录因子调控,在肝脏和白色脂肪组织中受高脂饮食抑制。这一途径的意义在于为细胞核提供“即用型”巴豆酰辅酶A,直接支持组蛋白的巴豆酰化修饰。
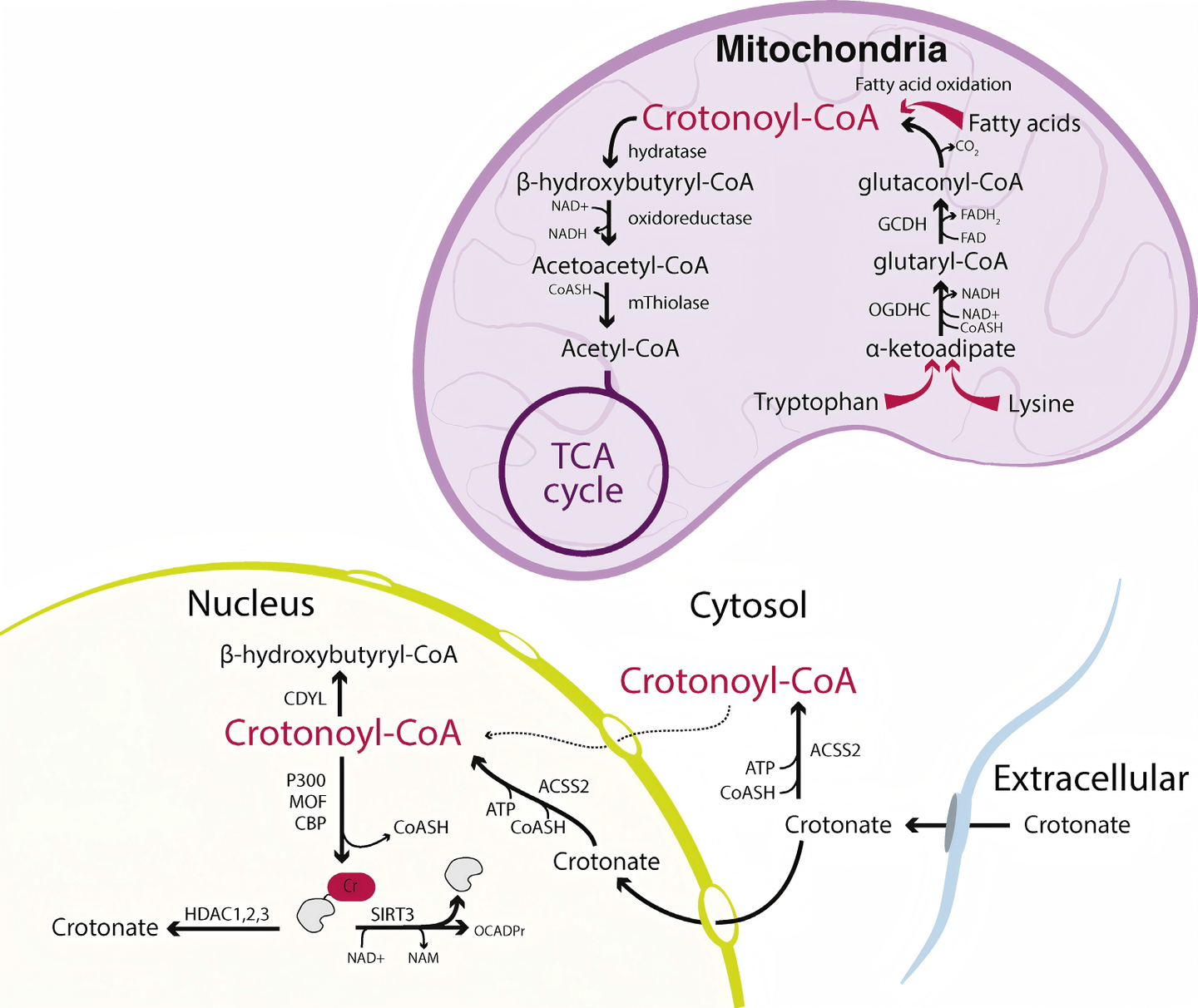
2.3 细胞区室化分布与转运
巴豆酰辅酶A的合成与利用呈现出明显的细胞区室化特征。线粒体是巴豆酰辅酶A生成的主要场所,这源于脂肪酸氧化和氨基酸分解代谢均发生于此。然而,组蛋白巴豆酰化修饰发生在细胞核内,因此需要将巴豆酰辅酶A或其前体从线粒体转运至核内。
目前认为存在两种可能的机制:一是巴豆酸形式的转运,即巴豆酸可从线粒体输出,进入胞浆和核内后被ACSS2重新活化为巴豆酰辅酶A;二是巴豆酰辅酶A的直接转运,但其具体机制尚不明确。值得注意的是,核内定位的CDYL(chromodomain Y-like transcription corepressor)具有巴豆酰辅酶A水合酶活性,可将巴豆酰辅酶A转化为β-羟基丁酰辅酶A,从而负向调控组蛋白巴豆酰化水平。这一发现提示,核内存在独立的巴豆酰辅酶A代谢调控机制。
2.4 与乙酰辅酶A的竞争关系
巴豆酰辅酶A与乙酰辅酶A在细胞内存在代谢竞争关系。尽管巴豆酰辅酶A丰度远低于乙酰辅酶A(通常不足后者的5%),但二者共享相同的酰基转移酶(如p300/CBP)。实验表明,降低乙酰辅酶A水平(如敲低ATP柠檬酸裂解酶ACL或丙酮酸脱氢酶PDH)可导致H3K18巴豆酰化水平升高,提示二者在酶活性中心存在底物竞争。这种竞争关系在营养缺乏条件下可能具有重要生理意义:当乙酰辅酶A供应不足时,巴豆酰辅酶A介导的修饰可维持关键基因的转录活性。
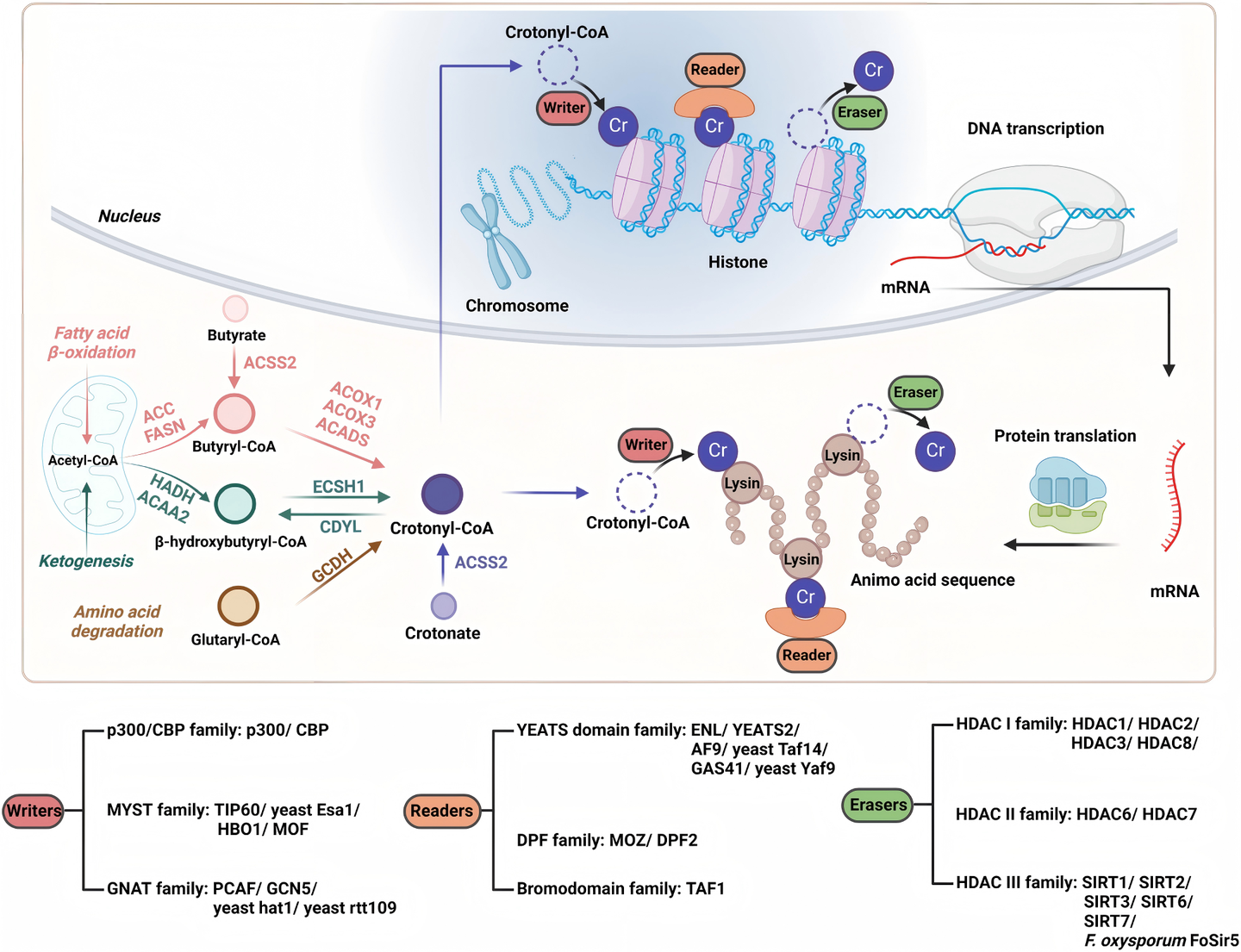
3. 巴豆酰化修饰系统
巴豆酰化修饰的动态平衡由三类功能蛋白共同维持:“写入器”(writers,巴豆酰转移酶)催化修饰添加;“擦除器”(erasers,去巴豆酰化酶)移除修饰;“阅读器”(readers)特异性识别修饰位点并传递信号。
3.1 巴豆酰转移酶
p300/CBP家族:p300和CBP是最早被发现并确认具有巴豆酰转移酶活性的蛋白质。Sabari等证明,p300能够以巴豆酰辅酶A为底物催化组蛋白H3K18巴豆酰化,且在无细胞转录体系中,p300介导的巴豆酰化比乙酰化更有效地激活转录。结构分析显示,p300的活性中心可容纳巴豆酰基链,但其巴豆酰转移酶活性较乙酰转移酶活性低约64倍。尽管如此,巴豆酰化对转录的激活效应却更为显著,这一悖论提示可能存在特定的识别机制增强了其功能输出。
MYST家族:MOF(KAT8)被证实具有巴豆酰转移酶活性,可催化H3K4、H3K9、H3K18、H3K23、H4K8和H4K12位点的巴豆酰化。其酵母同源物Esa1同样具有该活性,表明这一功能在进化上保守。
GNAT家族:GCN5在形成Gcn5-Ada2-Ada3(ADA)复合体后,可催化组蛋白H3和H5的巴豆酰化。有趣的是,单独的重组GCN5蛋白缺乏HCT活性,提示复合体组装对其功能至关重要。
其他转移酶:近年研究还发现,HBO1可催化H3K14cr和H4K12cr,TIP60介导EB1的K66巴豆酰化参与有丝分裂调控。值得注意的是,在蓝细菌中鉴定出的cGNAT2是首个在原核生物中确认的赖氨酸巴豆酰转移酶,其与乙酰辅酶A和巴豆酰辅酶A的结合位点存在空间差异,且催化两类反应的活性位点互不重叠,这为研究巴豆酰化的差异化调控机制提供了新视角。
3.2 擦除器:去巴豆酰化酶
I类HDACs:HDAC1、HDAC2和HDAC3被证实是主要的组蛋白去巴豆酰化酶。在小鼠胚胎干细胞中敲除HDAC1/2可使整体组蛋白巴豆酰化水平升高,总去巴豆酰化酶活性降低85%。HDAC3与NCoR1形成的复合体同样具有去巴豆酰化活性,且可被HDAC抑制剂(如伏立诺他、丁酸盐)抑制。
Sirtuins家族:SIRT1、SIRT2和SIRT3可在体外水解巴豆酰化组蛋白肽段,SIRT3的细胞内去巴豆酰化功能也已得到证实。此外,SIRT6可调控H3K27cr水平,SIRT7则介导PHF5A的K25去巴豆酰化参与衰老调控。
其他去酰化酶:在蓝细菌中发现的CddA是首个在原核生物中确认的去巴豆酰化酶,其对光系统I亚基PsaD的K108位点特异性去巴豆酰化调控光合作用效率,拓展了我们对这一修饰系统进化保守性的认识。
3.3 阅读器:巴豆酰化识别蛋白
YEATS结构域:YEATS结构域是目前研究最深入的巴豆酰化阅读器。TAF14的YEATS结构域优先识别H3K9cr,AF9识别H3K9cr、H3K18cr和H3K27cr,YEATS2特异性识别H3K27cr但不识别其他位点。这些YEATS结构域对巴豆酰化的亲和力显著高于乙酰化和丁酰化,反映了其识别长链酰基的偏好性。
DPF结构域:MOZ和DPF2的双PHD手指结构域可选择性识别H3K14cr,但不识别H3K9cr、H3K18cr或H3K27cr。这种位点特异性提示不同阅读器可能介导差异化的下游信号传递。
Bromodomain:溴结构域如TAF1也可结合巴豆酰化修饰,但亲和力低于乙酰化。
3.4 其他调控因子
CDYL:作为巴豆酰辅酶A水合酶,CDYL将巴豆酰辅酶A转化为β-羟基丁酰辅酶A,从而消耗底物、负向调控巴豆酰化水平。CDYL可调控H2BK12、H3K9、H3K27、H4K8等多个位点的巴豆酰化,参与精子发生和DNA损伤修复。
ACSS2:除合成巴豆酰辅酶A外,ACSS2本身也参与表观调控。在HIV潜伏期研究中,ACSS2介导的组蛋白巴豆酰化可逆转病毒潜伏状态。
代谢酶:ACADS、ACOX3、GCDH等通过调控巴豆酰辅酶A的生成间接影响巴豆酰化水平。
4. 巴豆酰化修饰的生物学功能
4.1 基因转录调控
巴豆酰化与转录活跃染色质区域高度重合。在小鼠精子细胞中,组蛋白巴豆酰化富集于性染色体上活性基因的启动子和增强子区域,调控精子发生过程中的基因表达。在巨噬细胞中,巴豆酸盐处理可增强炎症相关基因的转录响应。与乙酰化相比,巴豆酰化在基因启动子区域的分布更为集中,且对转录的激活效应更为持久。
值得注意的是,巴豆酰化在某些情境下也参与转录抑制。长链非编码RNA NEAT1通过结合p300/CBP复合体,调控内吞相关基因启动子区域的H3K27cr和H3K27ac平衡,从而抑制其转录。这种双向调控能力反映了巴豆酰化在不同染色质环境和阅读器背景下的功能多样性。
4.2 DNA损伤修复
巴豆酰化在DNA损伤应答中发挥多重作用。DNA双链断裂位点附近的组蛋白巴豆酰化水平显著降低,这一过程由CDYL1介导——CDYL1募集至断裂位点后发挥巴豆酰辅酶A水合酶活性,抑制H3K9的巴豆酰化。但有趣的是,CDYL1在断裂后同源重组修复中并非必需。
在非组蛋白层面,DNA损伤可诱导复制蛋白A1(RPA1)的K88、K379和K595位点巴豆酰化水平升高,增强其与单链DNA的结合能力,促进同源重组修复。此外,GCN5介导DNA依赖性蛋白激酶催化亚基(DNA-PKcs)的巴豆酰化,通过非同源末端连接(NHEJ)途径促进双链断裂修复。
4.3 细胞周期与增殖
巴豆酰化水平在细胞周期中呈现动态变化。在G1期阻滞的细胞中,组蛋白巴豆酰化水平较低;进入S期和G2/M期后显著升高。这一周期依赖性调控部分由I类HDACs介导——MS275抑制HDACs后,G1期细胞中巴豆酰化水平的下降被逆转。
在细胞增殖调控中,巴豆酰化的作用具有细胞类型特异性。在肝细胞肝癌中,提高整体巴豆酰化水平可抑制肿瘤细胞增殖和侵袭;而在宫颈癌HeLa细胞中,p300介导的HNRNPA1巴豆酰化反而增强细胞增殖、侵袭和迁移能力。这种差异性提示巴豆酰化的功能需要结合底物蛋白背景进行解读。
4.4 干细胞分化与发育
巴豆酰化在胚胎干细胞分化和早期发育中发挥关键作用。在小鼠胚胎干细胞中,Hdac1介导的组蛋白巴豆酰化影响Sox2、Oct4和Nanog等多能性因子的表达,促进胚层谱系基因的激活。在人多能干细胞向内胚层分化过程中,H4K77和H4K91的巴豆酰化水平显著升高,外源性巴豆酸盐处理可抑制多能性基因而促进内胚层标志基因表达。
在神经系统发育中,H3K9cr富集于活跃启动子区域,调控神经干/祖细胞的代谢和增殖相关基因。巴豆酰化可激活二价启动子(bivalent promoters),通过增加染色质开放性和募集RNA聚合酶II促进神经元分化。
4.5 代谢调控
巴豆酰化与细胞代谢状态形成双向调控环路。一方面,巴豆酰辅酶A的供应受脂肪酸氧化、氨基酸分解等代谢通路影响,使修饰水平反映细胞能量状态;另一方面,巴豆酰化可调控代谢关键酶的活性。在肝细胞肝癌中,GCDH通过降低巴豆酰化水平抑制磷酸戊糖途径和糖酵解,诱导细胞衰老并重塑抗肿瘤微环境。在白色脂肪棕色化过程中,二氢硫辛酰胺脱氢酶(DLD)的巴豆酰化通过RAS/ERK通路激活线粒体功能,促进产热。
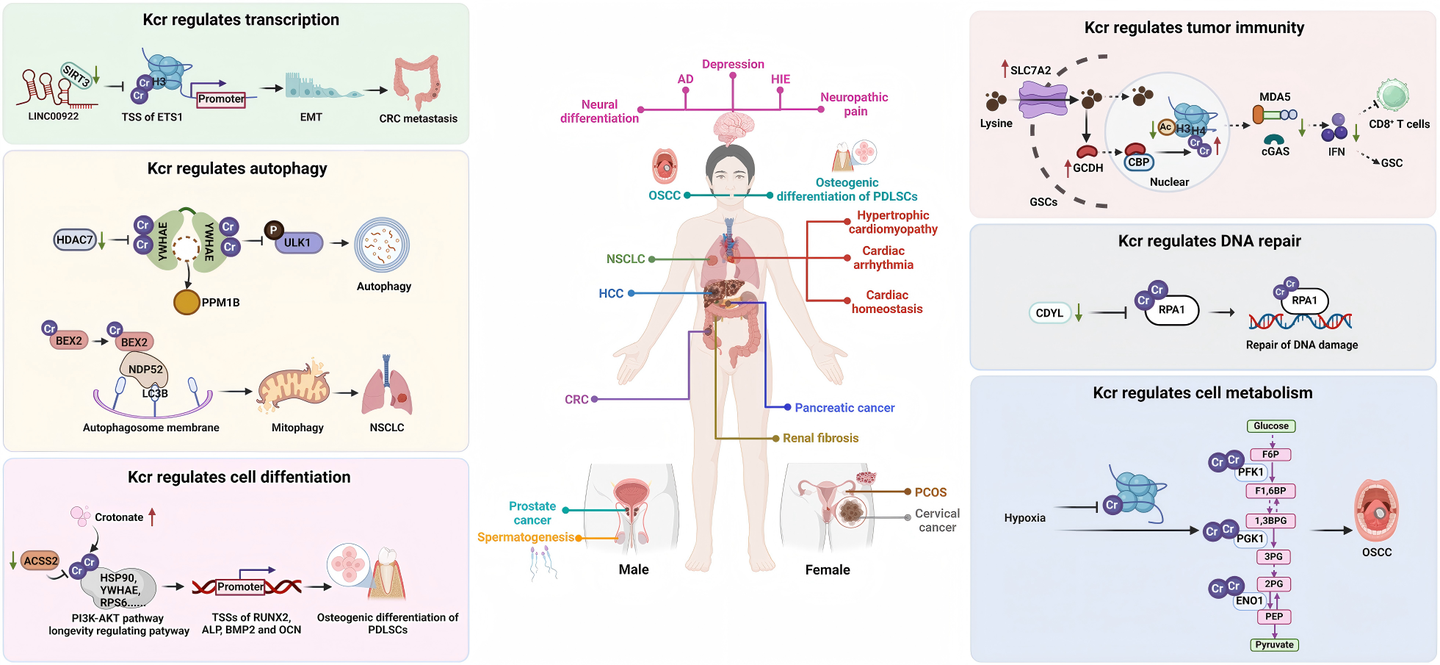
5. 巴豆酰化在疾病中的作用
5.1 肿瘤
5.1.1 肝细胞肝癌
在肝细胞肝癌中,巴豆酰化水平与肿瘤TNM分期相关。敲除HDAC1/3或使用HDAC抑制剂提高组蛋白巴豆酰化水平可抑制肝癌细胞迁移和增殖。Septin 2(SEPT2)的K74巴豆酰化在高度侵袭性细胞中显著上调,该位点的去修饰突变可损害SEPT2的GTP酶活性并抑制体内外转移。相反,HDAC6在缺氧条件下下调,导致lamin A的K265/270巴豆酰化升高,促进肝癌增殖。
5.1.2 结直肠癌
结直肠癌中巴豆酰化的研究最为广泛。H3K27cr水平在DNA损伤后降低,这一过程可能由SIRT6介导。ENO1的K420巴豆酰化由CBP催化、SIRT2去除,该修饰通过增强ENO1活性和调控肿瘤相关基因表达促进结直肠癌细胞生长、迁移和侵袭。LINC00922通过隔离SIRT3,上调ETS1启动子区域的H3K27cr水平,激活ETS1转录进而促进转移。值得注意的是,外周血单核细胞中的H2BK12cr水平可作为区分结直肠癌患者与健康对照的潜在生物标志物。
5.1.3 其他肿瘤
在非小细胞肺癌中,BEX2的K59巴豆酰化增强其与NDP52的相互作用,促进线粒体自噬并抑制化疗诱导的细胞凋亡。在前列腺癌中,H3K18cr水平与病理分级密切相关,BRD4抑制剂I-BET762可通过下调p300和巴豆酰化水平抑制肿瘤细胞增殖迁移。在胰腺癌中,MTHFD1的K354/K553去巴豆酰化通过增加铁死亡抵抗促进肿瘤进展。
5.2 神经系统疾病
在阿尔茨海默病中,NEAT1下调导致内吞相关基因启动子区域H3K27cr和H3K27ac失衡,影响Aβ清除。在抑郁症模型中,CDYL介导的组蛋白巴豆酰化通过转录抑制神经肽VGF影响突触可塑性,敲除前边缘皮质CDYL可缓解慢性社交 defeat 应激诱导的抑郁样行为。在缺氧缺血性脑病中,SB通过上调H3K9cr恢复神经营养因子表达,减轻脑损伤。
5.3 心血管疾病
在心肌肥厚中,NAE1的K236/K251双位点巴豆酰化水平升高,通过调控gelsolin的neddylation修饰影响心肌细胞生长。在缺血再灌注损伤中,增强心肌细胞巴豆酰化可改善心肌功能。SERCA2a的K120巴豆酰化在SIRT1心肌特异性敲除小鼠中与心功能障碍和心律失常相关。短链烯酰辅酶A水合酶ECHS1通过介导H3K18cr和H2BK12cr参与心脏稳态维持。
5.4 肾脏疾病
在急性肾损伤中,组蛋白巴豆酰化水平升高,通过上调PGC-1α和SIRT3、下调CCL2发挥肾脏保护作用。在肾纤维化中,ACSS2介导的H3K9cr促进IL-1β依赖性巨噬细胞活化和肾小管细胞衰老,抑制ACSS2可延缓纤维化进程。在常染色体显性多囊肾病中,CDYL下调导致H3K18cr升高加速囊肿生长。
5.5 生殖系统疾病
巴豆酰化在精子发生中发挥关键作用。组蛋白巴豆酰化富集于减数分裂后精子细胞的性染色体上,标记逃避X染色体失活的睾丸特异性基因。CDYL转基因小鼠中组蛋白巴豆酰化水平降低,伴有附睾精子计数和活力下降。在多囊卵巢综合征中,LONP1的K390去巴豆酰化与线粒体功能障碍和氧化应激相关。
5.6 代谢性疾病
在2型糖尿病中,LncRNA EPB41L4A-AS1通过GCN5介导GLUT4启动子区域H3K27cr抑制葡萄糖摄取。在糖尿病肾病中,巴豆酸盐处理可降低血糖和血清脂质水平,减轻炎症和纤维化损伤。在肥胖模型中,7,254个巴豆酰化位点被鉴定,涉及甘油-3-磷酸脱氢酶1、脂肪酸结合蛋白4等多个代谢酶的修饰调控白色脂肪棕色化。
5.7 感染性疾病
在HIV潜伏期,ACSS2介导的组蛋白巴豆酰化可逆转病毒潜伏状态。非经典NF-κB通路激活后,巴豆酰化增强p52亚基功能,促进HIV潜伏逆转。黄芩素通过抑制p300表达降低HIV启动子区域组蛋白巴豆酰化,从而抑制潜伏病毒再激活。
6. 结语
随着高分辨率蛋白质质谱技术的发展,研究发现巴豆酰化(Kcr)修饰不仅存在于组蛋白,也广泛存在于非组蛋白中,凸显了其在神经系统、代谢疾病及肿瘤发生等多系统疾病中的关键作用。尽管部分调控机制已被阐明,但由于Kcr调控因子与其他酰化修饰因子存在重叠,使得特异性调控网络的研究变得复杂,目前仍缺乏明确的特异性靶点。未来需在机制研究的基础上,结合临床试验,以全面解析Kcr的作用过程,为其相关疾病的防治提供潜在靶点。
参考文献
1. Ji, Y. et al. Lysine crotonylation in disease: mechanisms, biological functions and therapeutic targets. Epigenetics & Chromatin 18, 13 (2025).
2. Trefely, S., Lovell, C. D., Snyder, N. W. & Wellen, K. E. Compartmentalised acyl-CoA metabolism and roles in chromatin regulation. Molecular Metabolism 38, 100941 (2020).
3. Fellows, R. et al. Microbiota derived short chain fatty acids promote histone crotonylation in the colon through histone deacetylases. Nat Commun 9, 105 (2018).
4. 刘芳远, 苏丽娅. 巴豆酰化修饰在恶性肿瘤中的研究进展[J]. 肿瘤防治研究, 2023, 50(2): 195-201. DOI: 10.3971/j.issn.1000-8578.2023.22.0770




