什么是脂肪从头合成?
脂肪从头合成(de novo lipogenesis, DNL)是机体利用碳水化合物、氨基酸等非脂类碳源,经多步酶促反应合成脂肪酸的代谢途径,是连接糖代谢与脂质代谢的关键枢纽,在能量稳态维持、膜脂合成、信号分子产生等生理过程中发挥核心作用,其异常调控与肥胖、2型糖尿病、非酒精性脂肪性肝病(NAFLD)、肿瘤等多种疾病的发生发展密切相关。
DNL的代谢过程
1. 碳源摄取与核心前体生成
DNL的碳源主要来自循环中的碳水化合物,也可由谷氨酰胺、乳酸、乙酸、果糖等供给:
葡萄糖经糖酵解生成丙酮酸,进入线粒体后转化为草酰乙酸;同时,丙酮酸脱羧生成乙酰辅酶A。草酰乙酸与乙酰辅酶A在柠檬酸合酶催化下缩合生成柠檬酸。柠檬酸通过线粒体膜上的转运蛋白进入胞质,随后被ATP柠檬酸裂解酶(ACLY) 裂解生成乙酰辅酶A,这是DNFAS最主要的直接前体。
乙酸可通过胞质乙酰辅酶A合成酶2(ACSS2)直接生成乙酰辅酶A;
果糖经果糖激酶代谢后绕过糖酵解限速酶磷酸果糖激酶-1(PFK-1),更高效地生成乙酰辅酶A;
谷氨酰胺、乳酸可通过各自代谢途径进入TCA循环(谷氨酰胺→α-酮戊二酸;乳酸→丙酮酸),最终转化为柠檬酸,为DNL提供碳源。
2. 胞质内脂肪酸核心合成步骤
该过程发生在胞质中,由两个关键限速酶催化,最终生成DNL的核心终产物棕榈酸:
第一步限速反应:乙酰辅酶 A 在乙酰辅酶 A 羧化酶 1(ACC1) 催化下,经ATP供能羧化生成丙二酰辅酶A。
链延长循环:脂肪酸合酶(FASN) 作为同源二聚体,包含多个酶活性中心,以乙酰辅酶A为引物,丙二酰辅酶A为二碳供体,通过缩合-还原-脱水-再还原的4步循环,每次为脂肪酸链延长2个碳原子;经过7轮循环后,最终生成16碳的饱和脂肪酸棕榈酸(C16:0)。
3. 棕榈酸的下游代谢流延伸
DNL合成的棕榈酸并非代谢终点,而是通过延长反应和去饱和反应进一步代谢,生成机体所需的各类长链/超长链脂肪酸,这也是DNL代谢网络的重要组成部分:
脂肪酸延长:由超长链脂肪酸延长酶家族(ELOVL1-7)催化,以丙二酰辅酶A为二碳供体,在棕榈酸基础上继续延长碳链,可生成18~26碳的长链/超长链饱和脂肪酸(如硬脂酸C18:0、花生酸C20:0)。
脂肪酸去饱和:由去饱和酶家族催化,在脂肪酸链中引入双键,生成不饱和脂肪酸:硬脂酰辅酶A去饱和酶(SCD1/5):在Δ9位引入双键,将棕榈酸(C16:0)转化为棕榈油酸(C16:1n7)、硬脂酸(C18:0)转化为油酸(C18:1n9);
脂肪酸去饱和酶(FADS1/2):在Δ5/Δ6位引入双键,对膳食来源的必需脂肪酸(如亚油酸C18:2n-6,α-亚麻酸C18:3n-3) 进行进一步的加工,生成花生四烯酸(ARA,C20:4n-6)、二十碳五烯酸(EPA,C20:5n-3)等长链多不饱和脂肪酸,是调节膜磷脂组成和合成信号分子的核心途径。
DNL的组织特异性
1. 肝脏
肝脏是机体响应营养过剩的DNL器官。生理状态下,肝脏DNL仅在高碳水饮食后显著激活,合成的脂肪酸主要用于组装极低密度脂蛋白(VLDL),分泌到循环中供外周组织摄取利用,少量储存为肝内甘油三酯。病理状态下,肥胖、胰岛素抵抗、NAFLD患者的肝脏DNL发生异常亢进:健康人肝脏DNL仅贡献 2%~5% 的肝内甘油三酯,而NAFLD患者中这一比例高达 26%,是肝脂肪变性的核心驱动因素。同时,在胰岛素抵抗状态下,肝脏呈现选择性胰岛素抵抗:对胰岛素抑制糖异生的通路发生障碍,却保留了胰岛素促进DNL的效应,形成高血糖、高胰岛素血症与高甘油三酯血症并存的恶性循环。
2. 脂肪组织
脂肪组织是人类DNL的另一核心场所,高碳水饮食下,人体脂肪组织的总DNL合成量远超肝脏。根据脂肪类型不同,其功能存在显著差异:
白色脂肪组织(WAT):DNL主要由ChREBP驱动(ChREBP可以靶向并转录激活DNFAS全通路的所有关键限速酶),合成的脂肪酸主要用于自身甘油三酯储存,同时生成棕榈油酸、脂肪酸羟基脂肪酸酯(FAHFAs)等胰岛素增敏脂因子(lipokine),调控全身代谢稳态。肥胖、胰岛素抵抗状态下,WAT的DNL显著下调,lipokine生成减少,进一步加重全身胰岛素抵抗。
棕色脂肪组织(BAT):基础DNL活性远高于WAT,冷刺激可显著诱导其DNL激活,主要参与细胞内脂质储存和产热优化。但因BAT总量有限,其对全身DNL总量的贡献较小,其生理意义更多体现在通过产热消耗能量,而非向全身供应脂质。
3. 其他组织
肿瘤细胞:绝大多数实体瘤(肺癌、乳腺癌、前列腺癌等)均存在DNL通路的异常激活,FASN、ACC1等关键酶高表达,即使在外界脂质充足的情况下,仍通过DNL合成脂肪酸,满足肿瘤细胞快速增殖的膜合成需求。
泌乳期乳腺:DNL高度激活,合成的脂肪酸是乳汁脂肪的主要来源。
免疫细胞:T细胞、巨噬细胞活化时会显著上调DNL,满足细胞增殖和效应功能的代谢需求。
DNL的生理功能与病理意义
1. 生理功能
能量稳态调控:将饮食中过剩的碳水化合物转化为脂肪酸储存,避免高血糖引发的细胞毒性,是机体处理过剩能量的核心途径。
生物膜结构维持:DNL为细胞增殖、分化提供磷脂合成的脂肪酸前体,调控细胞膜的流动性、完整性和信号转导功能。
信号分子生成:DNL合成的脂肪酸是棕榈油酸、FAHFAs等lipokine的前体,这些分子可改善全身胰岛素敏感性、抑制炎症、调控产热,是脂肪-肝脏-肌肉器官间对话的关键信使。
脂肪酸多样性生成:通过碳链延长和去饱和反应,将棕榈酸转化为油酸(C18:1n9)、棕榈油酸(C16:1n7)等单不饱和脂肪酸,以满足细胞对特定酰基链结构的需求。
2. 异常DNFAS相关疾病
代谢性疾病:肝脏DNL异常亢进是NAFLD、2型糖尿病、高脂血症的核心发病机制之一;而脂肪组织DNL下调会加剧胰岛素抵抗和全身代谢紊乱。
恶性肿瘤:DNL通路异常激活是肿瘤的标志性代谢特征,FASN高表达与肿瘤的增殖、侵袭、转移及不良预后密切相关。
免疫与炎症性疾病:T细胞、巨噬细胞的DNL异常会影响其活化和效应功能,参与自身免疫病、慢性炎症的发生发展;病毒感染时,宿主细胞的DNL通路会被病毒劫持,用于病毒包膜的合成,是抗病毒治疗的潜在靶点。
]服务简介
代谢流(Metabolic flux)是细胞生理学的一个基本的决定因素,在稳态条件下,代谢流量一般以代谢产物的比生成速率表示,是代谢途径中最重要的参数。代谢流量分析(Metabolic flux analysis,MFA)是根据代谢路径中各个反应的计量关系以及实验中所测得的数据,来确定整个代谢反应网络中代谢流量分布的一种分析方法。代谢流量组学(Fluxomics)是研究代谢流量组(Fluxome)随时间动态变化的科学,即对流经代谢途径的代谢流量组进行定量分析。分子流量变化反映了遗传和代谢调控的综合结果,决定了细胞表型。因此转录组学、蛋白质组学和代谢组学提供了代谢网络容量和热动力学测试,而代谢流量组学则是对通过网络中每步反应的流量值进行精细定量,可以认为是对代谢表型的直接衡量。MFA和Fluxomics分析尤其是基于 13C 标记的 Fluxomics 技术已成为近年来的研究热点技术之一,在肿瘤、糖尿病、植物和微生物工程研究中大放异彩。
]实验设计流程
基于稳定性同位素标记底物的代谢流组学实验对象一般为动物模型样本和细胞模型样本,一般实验流程如下 :

代谢流量组学是代谢组学的精细化技术,在功能基因组研究中发挥着举足轻重的作用。通常会有这一现象出现:虽然代谢流量发生了显著变化,但并没有引起相应代谢物水平甚至最终产物发生任何改变。在这种情况下必然存在某种调节机制发挥作用,为揭示基因功能提供重要的信息。因此,代谢流量组学是功能基因组研究的重要组成部分。
]同位素类型
基于13C、15N和2H 等稳定性同位素标记的代谢前体物:[1,2-13C2]-glucose, [U-13C6]-glucose, [U-13C5]-glutamine, [13C5,15N2]-glutamine, [13C4]-aspartic acid, [2,3,3-D3]-serine, [13C3,15N]-serine, [13C2,15N]-glycine, [U-13C6]-fructose, D2O
注:本公司常年备有如下所示的同位素标记前体物现货,供客户按需购买:
1. D-Glucose (U-13C6)
2. D-Glucose (1,2-13C2)
3. D-Glucose (1-13C)
4. L-Glutamine (13C5)
5. L-Glutamine (amine-15N)
6. L-Glutamine (1-13C)
7. L-Glutamine (5-13C)
]覆盖途径
谱领生物提供国际领先的多种途径代谢流组学分析服务,可满足多种代谢组学和表型组学研究要求:
1. 糖酵解途径(Glycolysis, or Embedn-Meyerhof-Parnas, EMP)
2. 三羧酸循环途径(Tricarboxylic Acid Cycle, TCA cycle)
3. 磷酸戊糖途径(Pentose Phosphate Pathway, PPP)
4. 糖异生(Gluconeogenesis)
5. 卡尔文循环(Calvin Cycle)
6. 脂肪酸从头合成 (de novo Fatty acid Synthesis)
7. 脂肪酸氧化代谢 (Fatty acid Oxidation)
8. 短链脂肪酸合成(Short-Chain Fatty acid Synthesis)
9. 一碳代谢之蛋氨酸循环(Methionine cycle in One-carbon Metabolism)
10. 一碳代谢之四氢叶酸循环(Tetrahydrofolate cycle in One-carbon Metabolism)
11. 核苷酸代谢 (Nucleotide Metabolism)
12. 谷胱甘肽合成代谢 (Glutathione Metabolism)
13. 支链氨基酸代谢(Branch-chain Amino Acid Catabolism)
14. 精氨酸代谢(Arginine Metabolism)
15. 色氨酸代谢 (Tryptophan Metabolism)
16. 尿素循环 (Urea Cycle)
17. NADPH 等能量代谢途径
* 不在以上途径的其他物质的定制类代谢流服务请详询谱领工作人员;
* 可以同时对多种同位素进行标记分析。
]可接受的样本类型
哺乳动物细胞(贴壁培养、悬浮培养、原代)、动物组织、微生物、植物细胞、植物组织、藻类、土壤等。
]服务流程

]样本量要求

]细胞模型样本

]生物学重复
相较于其他组学,代谢组学更加灵敏,更接近于真实情况。因此,为保证实验结果的可靠性,要求更多的生物学样本重复。我们建议:
动物样本,单组不少于9 例重复;
细胞、微生物样本,单组不少于5 例重复;
其他如植物样本,单组不少于7 例重复。
]仪器平台
平台一:超高效液相色谱高分辨质谱联用仪(UHPLC-HRMS)Q Exactive ™ ( Thermo Scientific Orbitrap MS)
使用 Thermo Scientific™ Q Exactive™ 组合型四极杆 Orbitrap 质谱仪可以快速可靠地识别、定量和确认更多化合物。 本台式 UHPLC-HRMS 系统将四极杆母离子选择性与高分辨率和准确质量数(HRAM)Orbitrap 检测相结合,提供出色性能和多功能性。 Q Exactive 质谱仪特别适用于非目标或目标化合物筛查,也能够实现广泛的定性和定量应用。

平台二:气相色谱质谱联用仪(GC-MS)7890A/5975C(Agilent GC-MS)
气相色谱- 质谱与生俱来的定量准确性( 无液相色谱- 质谱联用平台常用的电喷雾离子化所存在的基质抑制效应)、超高的稳定性和易用性,以及不俗的灵敏度和高通量,能胜任多数代谢组学和基础生命科学研究任务。尤其是那些浓度较高、具有挥发性的物质或虽具有亲水性但衍生后具有挥发性的代谢物,如短链脂肪酸、糖酵解和三羧酸循环相关代谢物、氨基酸和中长链脂肪酸等,都十分适用。

平台三:气相色谱飞行时间质谱联用仪(GC-Tof/MS)7890A/5975C(LECO Pegasus® HT)
Pegasus® HT 把高通量飞行时间质谱技术与ChromaTOF® 软件相结合,极大的提高了实验室效率及生产力。全质量范围500 张谱图每秒的采集速率大大缩短了分析时间。 Dynamic Signal Tracking (DST)大大提高了Pegasus 质谱的动态范围,全谱采集,系统可靠耐用,重复性好。独一无二的自动数据处理能力最简化枯燥的手工操作,增强数据质量。完全自动定性、定量分析,样品全分析时间周期大大快于常规手动分析。Pegasus HT 提供给您先进智能的数据挖掘算法,自动提取出通常无法识别的被基质或共流干扰物遮盖的化合物。

]服务示例

项目名称:脂肪酸代谢流物质列表 | |||
No | Metabolite | 简写 | 中文名 |
1 | Capric acid | FA(10:0) | 癸酸 |
2 | Lauric acid | FA(12:0) | 月桂酸 |
3 | Myristic acid | FA(14:0) | 肉豆蔻酸 |
4 | Myristoleic acid | FA(14:1n5t) | 肉豆蔻油酸 |
5 | Palmitic acid | FA(16:0) | 棕榈酸 |
6 | Palmitoleic acid | FA(16:1n7c) | 顺式棕榈油酸 |
7 | Stearic acid | FA(18:0) | 硬脂酸 |
8 | Oleic acid | FA(18:1n9c) | 油酸 |
9 | Linoleic acid | FA(18:2n6c) | 亚油酸 |
... ... | |||
17 | Erucic acid | FA(22:1n9c) | 芥酸 |
18 | Lignoceric acid | FA(24:0) | 二十四烷酸 |
19 | Docosahexaenoic acid | FA(22:6n3) | 顺式-4,7,10,13,16,19-二十二碳六烯酸 |
20 | Nervonic acid | FA(24:1n9) | 神经酸 |
详情请联系谱领生物工作人员,脂肪酸种类可根据实验需求进行个性化拓展。 | |||
CUL3-KLHL25 介导的 ACLY 泛素化诱导脂肪酸代谢重编程以促进 iTreg 分化
标题:CUL3-KLHL25 介导的 ACLY 泛素化诱导脂肪酸代谢重编程以促进 iTreg 分化
期刊:eLife
发表时间:2021年9月
研究内容
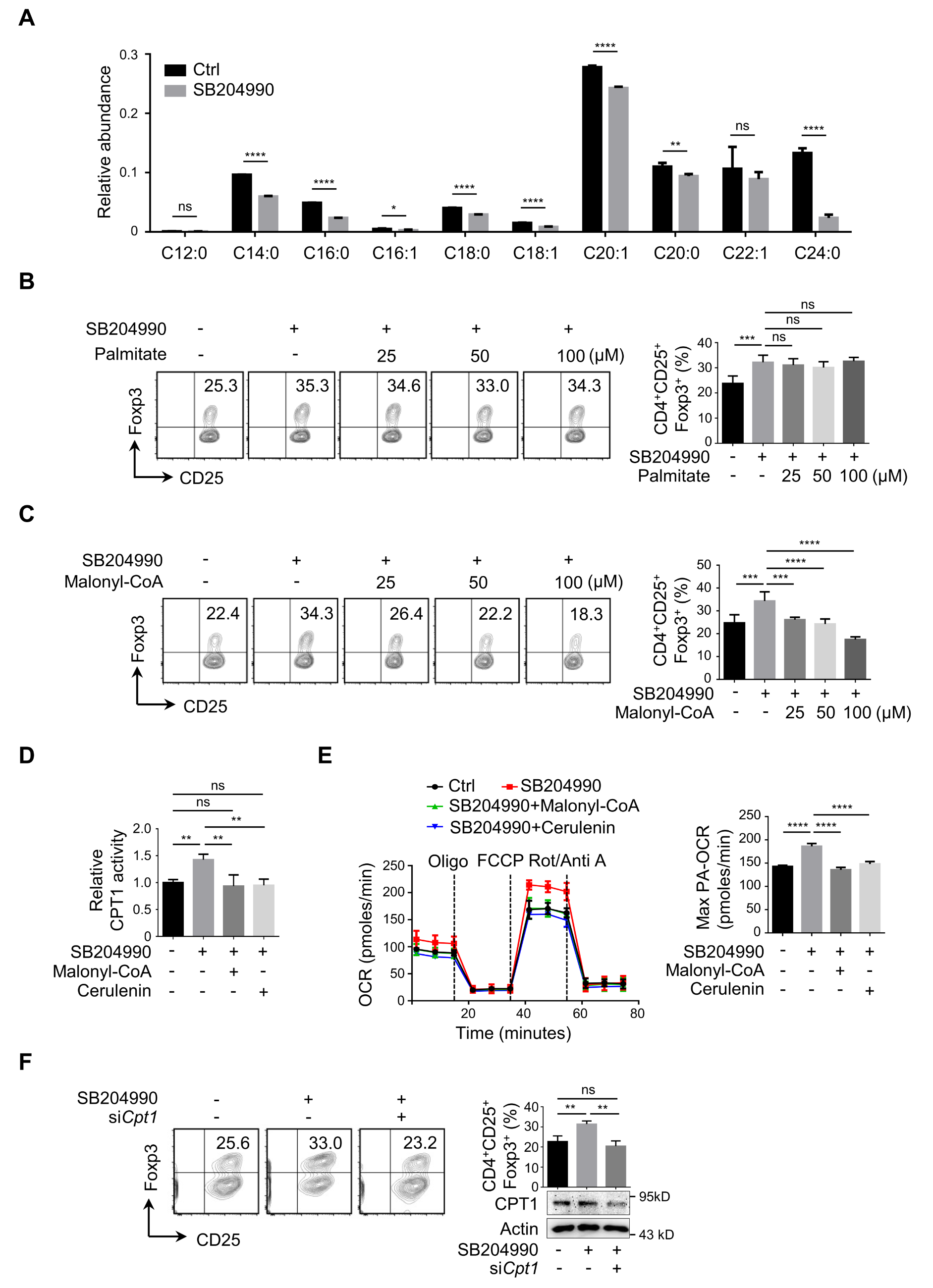
该研究揭示了诱导性调节性T细胞(iTreg)分化过程中脂肪酸代谢重编程的关键调控机制。研究发现,在转化生长因子β1(TGF-β1)刺激下,ATP-柠檬酸裂解酶(ACLY)的酶活性显著下降,这是由于CUL3-KLHL25复合物介导的ACLY泛素化降解所致。ACLY的降解导致脂肪酸合成中间产物丙二酰辅酶A水平降低,从而解除了其对脂肪酸氧化限速酶CPT1的抑制作用,最终通过增强脂肪酸氧化来促进iTreg分化。本文阐明了TGF-β1-CUL3-KLHL25-ACLY轴在调控iTreg分化中的重要作用,为理解免疫稳态维持及预防免疫性疾病提供了新视角。
材料与方法
该研究通过[U-13C]葡萄糖标记的脂肪酸代谢流实验,检测诱导性调节性T细胞(iTreg)中脂肪酸合成中的代谢物
结果
1. ACLY 是 iTreg 分化过程中脂肪酸代谢重编程的关键调控因子。
2. 13C标记的脂肪酸减少,说明抑制 ACLY 会减少脂肪酸合成(FAS),但甲羟戊酸-胆固醇合成途径及组蛋白乙酰化水平保持稳定,说明这些途径并非 ACLY 调控 iTreg 分化的主要机制。
3. 抑制 ACLY 会降低丙二酰辅酶A 水平,而外源性补充丙二酰辅酶A 则能完全消除 ACLY 抑制诱导的 iTreg 分化。
进一步的代谢流分析表明,ACLY 抑制导致的丙二酰辅酶A 减少,解除了其对 CPT1 的抑制作用,从而增强脂肪酸氧化(FAO),最终促进 iTreg 分化。
靶向ALOX12-ACC1的小分子改善小鼠和食蟹猴的非酒精性脂肪性肝炎
标题:靶向ALOX12-ACC1的小分子改善小鼠和食蟹猴的非酒精性脂肪性肝炎
期刊:SCIENCE TRANSLATIONAL MEDICINE
发表时间:2021年12月
研究内容
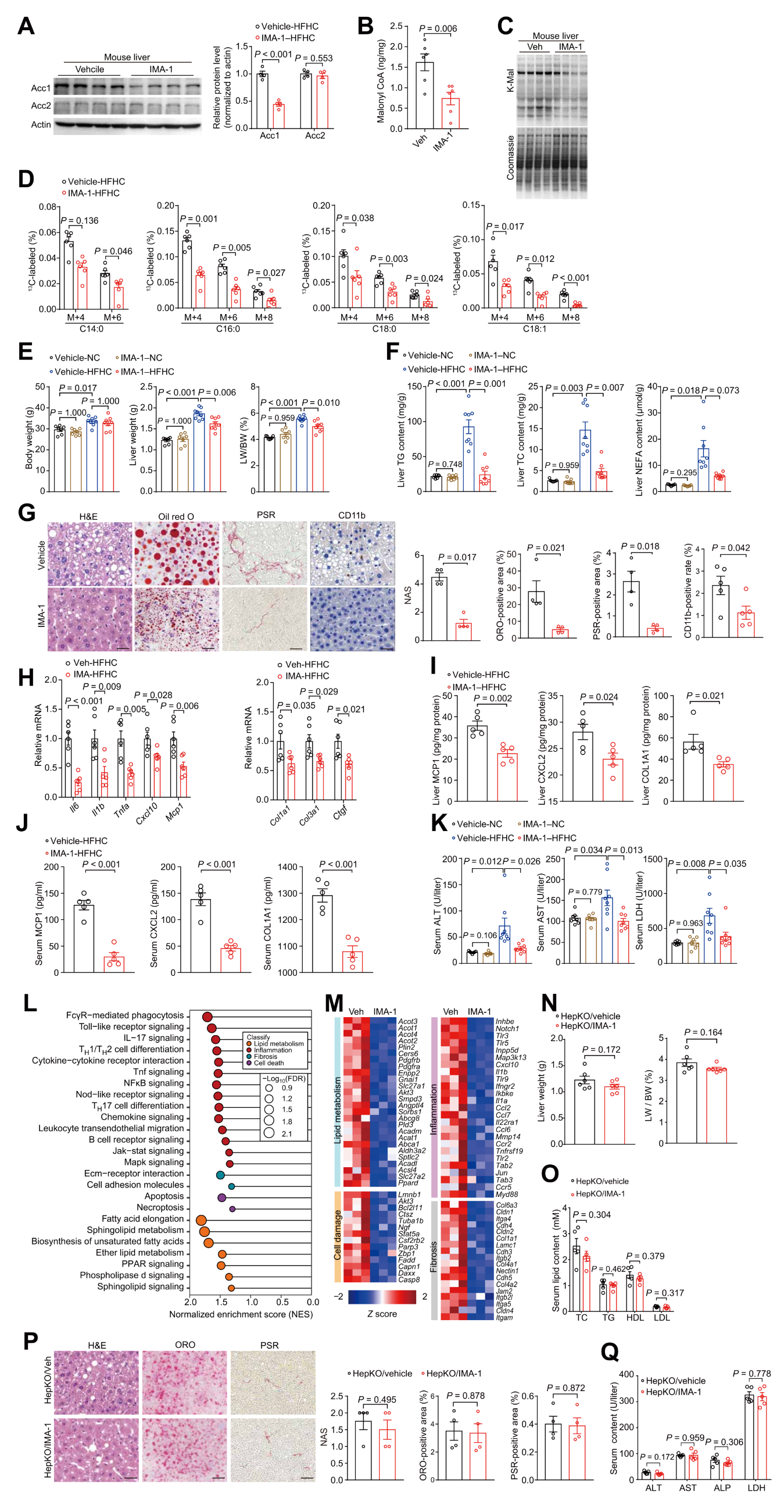
本研究报道了一种小分子化合物IMA-1,通过靶向ALOX12-ACC1相互作用治疗非酒精性脂肪性肝炎(NASH)。IMA-1直接结合ALOX12靠近ACC1结合界面的口袋,破坏两者互作,但不抑制ALOX12酶活性。在雄性小鼠和食蟹猴模型中,IMA-1均显著抑制饮食诱导的NASH进展,疗效与ACC抑制剂相当,且不引起高脂血症副作用。本研究为靶向ALOX12-ACC1界面的NASH治疗策略提供了跨物种概念验证。
材料与方法
小鼠经口服灌胃给予[1,2-13C]乙酸(Sigma公司)1 g/kg剂量。[1,2-13C]乙酸处理24小时后处死小鼠,灌注后收集肝脏检测 13C标记脂肪酸的分布情况。
结果
研究团队采用[1,2-13C]乙酸钠进行体内示踪实验,检测肝脏中13C标记脂肪酸在总脂肪酸中的百分比,以此评估肝脏DNL速率。结果显示,IMA-1处理显著抑制了小鼠肝脏中的DNL代谢流,表明其通过调控脂肪酸合成途径发挥抗NASH作用。
参考文献
1. Tian, M. et al. ACLY ubiquitination by CUL3-KLHL25 induces the reprogramming of fatty acid metabolism to facilitate iTreg differentiation. eLife 10, e62394 (2021).
2. Zhang, X.-J. et al. A small molecule targeting ALOX12-ACC1 ameliorates nonalcoholic steatohepatitis in mice and macaques. Sci. Transl. Med. 13, eabg8116 (2021).





