丙酰辅酶 A:代谢-表观遗传交联的核心调控因子
丙酰辅酶A(Propionyl-CoA)作为一种关键的代谢中间产物,不仅参与机体的能量代谢过程,还深度参与组蛋白修饰和基因表达调控,是连接代谢与表观遗传的重要分子。
一、丙酰辅酶A的生成:代谢途径与区室化分布
丙酰辅酶A带有一个三碳的酰基基团,它的的生成并不是单一途径,而是来自多个代谢过程,且具有明显的“区室化”特点——也就是在细胞的不同部位(线粒体、过氧化物酶体、细胞质)分别生成,各自承担不同的代谢功能:
1. 线粒体:丙酰辅酶A生成的主要场所
线粒体是能量代谢的核心,也是丙酰辅酶A最主要的生成部位,多种底物的分解代谢都会最终汇聚到这里生成丙酰辅酶A,主要包括三类:
第一类是氨基酸代谢,比如甲硫氨酸、苏氨酸,还有两种支链氨基酸——异亮氨酸和缬氨酸,它们分解后会产生丙酰辅酶A;第二类是奇数链脂肪酸的氧化,奇数链脂肪酸氧化的终产物之一就是丙酰辅酶A;第三类是胆固醇侧链的氧化。线粒体中生成的丙酰辅酶A,最终会通过多步反应进入三羧酸循环(TCA循环),参与能量生成。第一步,在丙酰辅酶A羧化酶(PCC)的催化下,丙酰辅酶A羧化生成(S)-甲基丙二酰辅酶A;第二步,通过甲基丙二酰辅酶A差向异构酶,将(S)型转化为(R)型;第三步,在维生素B12依赖的甲基丙二酰辅酶A变位酶(MCM)催化下,最终转化为琥珀酰辅酶A,从而进入三羧酸循环。这三步反应是线粒体中丙酰辅酶A代谢的核心,也是“丙酸血症”的关键靶点。
2. 过氧化物酶体:丙酰辅酶A的次要生成部位
除了线粒体,过氧化物酶体也能生成丙酰辅酶A,主要是通过支链脂肪酸的氧化,比如我们饮食中来自反刍动物乳制品的植烷酸,它在过氧化物酶体中氧化后会产生丙酰辅酶A。过氧化物酶体中生成的丙酰辅酶A,不能直接跨膜运输,目前认为它有两种转运方式:要么被过氧化物酶体中的CrAT酶转化为丙酰肉碱,要么被过氧化物酶体中的硫酯酶转化为丙酸,然后通过PXMP2孔蛋白运输到细胞其他部位。
3. 细胞质:丙酰辅酶A的补充生成部位
细胞质中的丙酰辅酶A,主要来自短链脂肪酸——丙酸的转化,这个过程需要酰基辅酶A合成酶的参与。比如大鼠线粒体中的短链酰基辅酶A合成酶3(ACSS3),就优先利用丙酸作为底物,生成丙酰辅酶A;酵母中的乙酰辅酶A合成酶也能催化这个反应,只是对丙酸的亲和力不如对乙酸高。
tips:丙酸主要来自肠道菌群的代谢,它和乙酸、丁酸一起,是肠道和血液循环中最丰富的三种短链脂肪酸。不过丙酸大部分在肝脏中代谢,人体门静脉血中的丙酸浓度(17-194μM)远高于外周血(1-13μM)。另外,我们的饮食也会影响丙酸的生成——比如膳食纤维能调节肠道菌群,促进丙酸产生;丙酸还常作为食品添加剂(抗菌剂、调味剂),直接通过饮食摄入。
4. 丙酰辅酶A的跨膜运输:肉碱穿梭系统
丙酰辅酶A不能直接穿过线粒体内膜,它要运输到细胞质,必须依靠“肉碱穿梭系统”:首先在线粒体中,由CrAT酶将丙酰辅酶A转化为丙酰肉碱,丙酰肉碱可以跨膜进入细胞质,之后再在细胞质中重新转化为丙酰辅酶A。
这里有个临床相关的例子:如果患者有先天性代谢缺陷,导致PCC或MCM酶缺乏(也就是丙酸血症),线粒体中会积累大量丙酰辅酶A,进而导致丙酰肉碱水平升高2000倍——这也是临床诊断丙酸血症的一个重要指标。另外,细胞质中的丙酰辅酶A,可以被细胞质中的脂肪酸合成酶(FASN)利用,合成奇数链脂肪酸,这个过程也依赖CrAT酶。还有研究发现CrAT酶可以定位在细胞核中,能将乙酰肉碱转化为乙酰辅酶A,因此推测它可能也能为细胞核中的组蛋白丙酰化提供丙酰辅酶A。丙酰辅酶A主要在线粒体、过氧化物酶体、细胞质中生成,各部位的生成途径和转运方式不同,核心酶和底物来源也各有特点;虽然目前还不清楚,用于组蛋白修饰的丙酰辅酶A具体来自哪个代谢池,但CrAT酶很可能参与了它从线粒体到细胞质、细胞核的运输。
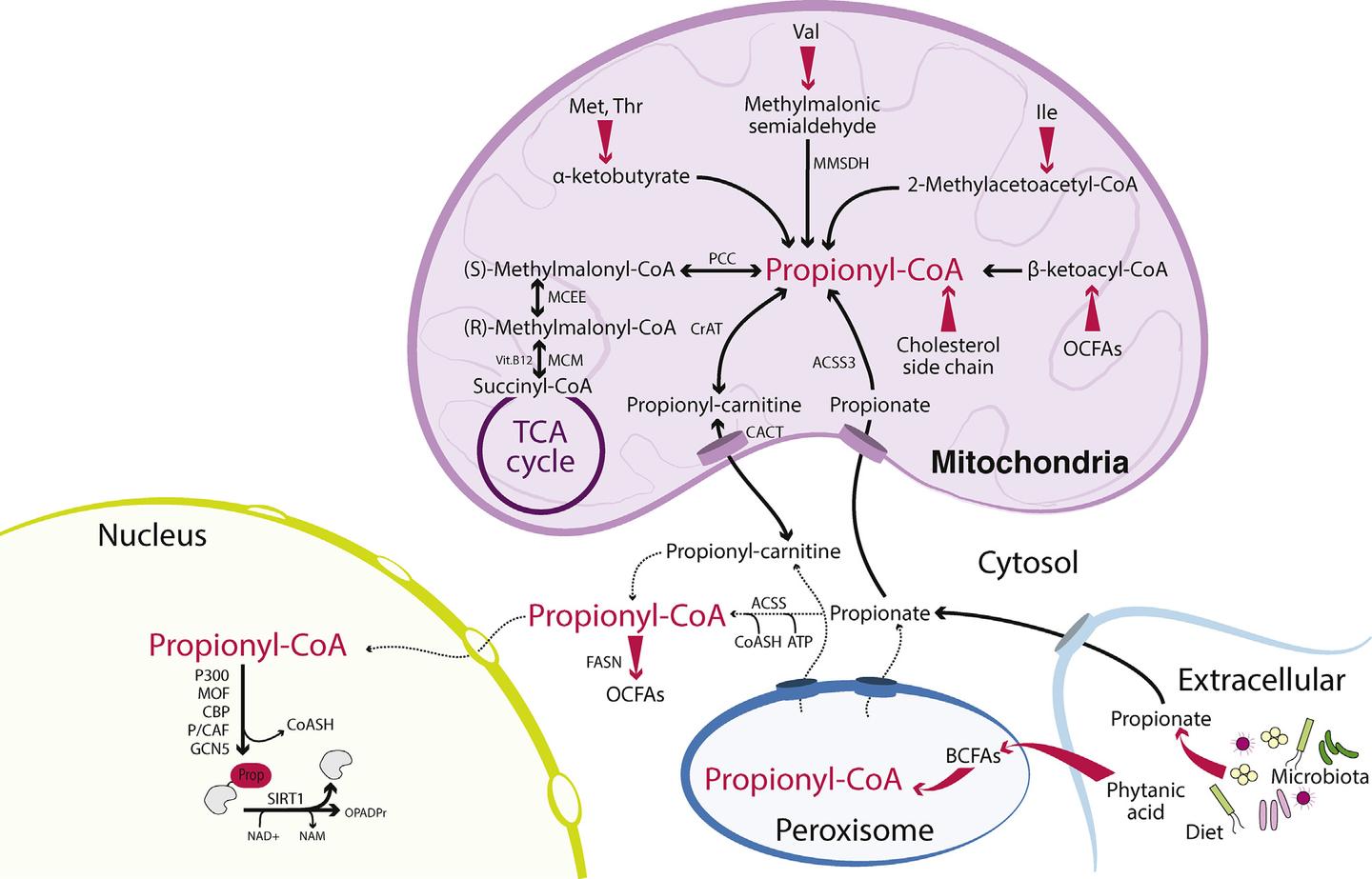
二、组蛋白赖氨酸丙酰化:作用与调控
丙酰辅酶A还有一个重要功能——参与组蛋白修饰,也就是“赖氨酸丙酰化(Kpr)”。组蛋白修饰是表观遗传的重要方式,通过改变染色质结构,调控基因表达。丙酰辅酶A作为“丙酰基团供体”,参与组蛋白赖氨酸残基的丙酰化。
1.组蛋白丙酰化的功能:激活基因转录
赖氨酸丙酰化最早是在组蛋白H3和H4上发现的,它的核心功能和赖氨酸乙酰化类似——都是“激活基因转录”。研究发现关键实验证据:通过ChIP-seq(染色质免疫沉淀测序)分析H3K14pr(组蛋白H3第14位赖氨酸丙酰化),发现31%的H3K14pr峰位于启动子-转录起始位点(TSS)区域;再结合RNA-seq数据,发现H3K14pr的丰度和基因表达水平呈正相关。另外,实验还发现:H3K14pr、H3K9Ac(乙酰化)、H3K14bu(丁酰化)常常出现在同一个基因位点上,说明这几种修饰可能协同作用,共同激活基因转录。更直接的证据来自无细胞体外转录系统:丙酰辅酶A可以替代乙酰辅酶A,刺激基因转录——这进一步证明了丙酰化对转录激活的作用。除了转录激活,组蛋白丙酰化还和细胞分化有关:在肌细胞分化过程中,组蛋白丙酰化水平会下降,同时丙酰辅酶A的水平也会下降;同样,U937白血病细胞在单核细胞分化过程中,H3K23位的丙酰化会消失。组蛋白丙酰化在维持细胞特性、调控分化中具体的功能的作用,还需要进一步研究证实。
2. 丙酰化的酶学调控:与乙酰化共用核心酶
组蛋白丙酰化的添加和去除,很多时候和乙酰化共用同一套酶,这也是它和乙酰化功能相似的重要原因。具体来说:添加丙酰基团的“酰基转移酶”,包括细菌中的GCN5相关乙酰转移酶、去乙酰化酶CobB,以及真核生物中的p300、CBP、P/CAF、GCN5、MOF等,这些酶不仅能催化乙酰化,也能催化丙酰化;而去除丙酰基团的“去酰基酶”,主要是SIRT1和SIRT2,同样也是乙酰化的去乙酰化酶。另外,组蛋白丙酰化的“读取蛋白”,也和乙酰化相似。通过肽段下拉实验发现,结合H3K14pr的蛋白,和结合H3K14Ac的蛋白非常相似,其中就包括(P)BAF染色质重塑复合物的组分——这些读取蛋白结合丙酰化位点后,会进一步调控染色质结构,促进基因转录。
组蛋白丙酰化由酰基转移酶催化添加、去酰基酶催化去除,与乙酰化共用核心酶,读取蛋白也相似,这决定了它和乙酰化在功能上可能存在重叠,核心都是激活基因转录。
3. 丙酰辅酶A的丰度:直接调控组蛋白丙酰化水平
组蛋白(以及非组蛋白)的丙酰化水平,和丙酰辅酶A的丰度密切相关。在分离的细胞核中,补充丙酰辅酶A会以“剂量依赖”的方式增加组蛋白丙酰化;同时,补充丙酰辅酶A会导致H3K14pr升高、H3K14Ac降低——这说明,丙酰化和乙酰化会竞争同一个酰基转移酶,当丙酰辅酶A充足时,会优先发生丙酰化,抑制乙酰化。虽然细胞中乙酰辅酶A的丰度是丙酰辅酶A的10-15倍,但在HeLA细胞和肌细胞中,H3K14Ac和H3K14pr的化学计量比却差不多——这说明,组蛋白丙酰化的水平,不仅仅取决于丙酰辅酶A的绝对丰度,可能还受到其他因素的调控(比如酶的特异性、染色质区域的可及性等)。临床案例再次印证了这一点:丙酸血症患者(PCC酶缺乏),线粒体中丙酰辅酶A无法正常代谢,导致其丰度显著升高,进而引起成纤维细胞中蛋白质丙酰化水平增加;同样,PCCα亚基缺陷的小鼠,肝脏中H3K14pr水平也会升高。另外,丙酰辅酶A在体内的分布也有差异,肝脏中含量最高,其次是肾脏、心脏、肌肉和大脑——这也提示,不同组织中组蛋白丙酰化的水平可能存在差异。
目前我们还不清楚细胞整体的丙酰辅酶A丰度(主要反映线粒体中的含量),和细胞核中的丙酰辅酶A丰度是否存在关联——这也是一个需要进一步研究的问题,但可以确定的是,丙酰化是一个动态调控的过程,且对代谢状态非常敏感。
4. 饮食、丙酰辅酶A与组蛋白丙酰化的相互作用
丙酸(丙酰辅酶A的前体)主要在肝脏和胃肠道代谢,而饮食摄入的丙酸,会显著影响肝脏代谢——比如影响脂质代谢、胰岛素敏感性、食欲和运动表现。丙酸补充剂的部分作用,可能是通过改变组蛋白丙酰化实现的。有研究发现,小鼠喂4周高脂饮食,肝脏和附睾白色脂肪中的丙酰辅酶A水平会下降;另一份研究发现,喂8周高脂饮食的小鼠,肝脏中H3K23pr水平会下降;但还有一份研究发现,喂12周高脂饮食的小鼠,肝脏中丙酰辅酶A水平会升高。出现这种差异的原因推测可能和高脂饮食的时长有关,也可能和肠道菌群的差异有关——因为肠道菌群产生短链脂肪酸(包括丙酸)的过程,会受到饮食的显著影响。所以,饮食如何通过调控丙酰辅酶A代谢,进而影响组蛋白丙酰化,还需要更多的研究来阐明机制。
丙酰辅酶A作为连接“代谢”和“表观遗传”的关键分子,其研究不仅能加深我们对代谢调控机制的理解,还可能为相关疾病(比如丙酸血症、代谢综合征、肿瘤等)的治疗,提供新的思路和靶点。




