Cell: 代谢流揭示线粒体“PEP穿梭”路径,解锁甘油异生全新调控通路
01 文章导读
长期以来,细胞如何生成并利用高能量的PEP分子,一直是代谢领域的基础科学问题。在糖异生和甘油异生过程中,PEP可通过两条途径合成:一条是胞质途径,由胞质型磷酸烯醇式丙酮酸羧激酶(PCK1,亦称C-PEPCK)催化;另一条是线粒体途径,由线粒体型磷酸烯醇式丙酮酸羧激酶(PCK2,亦称M-PEPCK)催化。过去的研究多聚焦于PCK1,尤其是其在肝脏糖异生中的作用。相比之下,PCK2虽在胰腺β细胞和脂肪组织中也有高表达,但其生理意义仍不清晰,特别是它在线粒体内生成的PEP如何被运送到胞质中参与合成代谢,一直是个悬而未决的关键问题。
由于线粒体内膜对大多数代谢物具有高度不通透性,PEP从线粒体输出必须依赖特定的载体蛋白。2026年3月17日,哈佛医学院 Shingo Kajimura 团队在《Cell》发表题为“Mitochondrial control of glycerolipid synthesis by a PEP shuttle”的研究论文,首次成功鉴定出SLC25A35是线粒体内膜上的PEP转运蛋白,从而填补了线粒体代谢物转运网络中的关键空白。

02 研究内容及结果
1. 参与PEP合成的线粒体载体蛋白
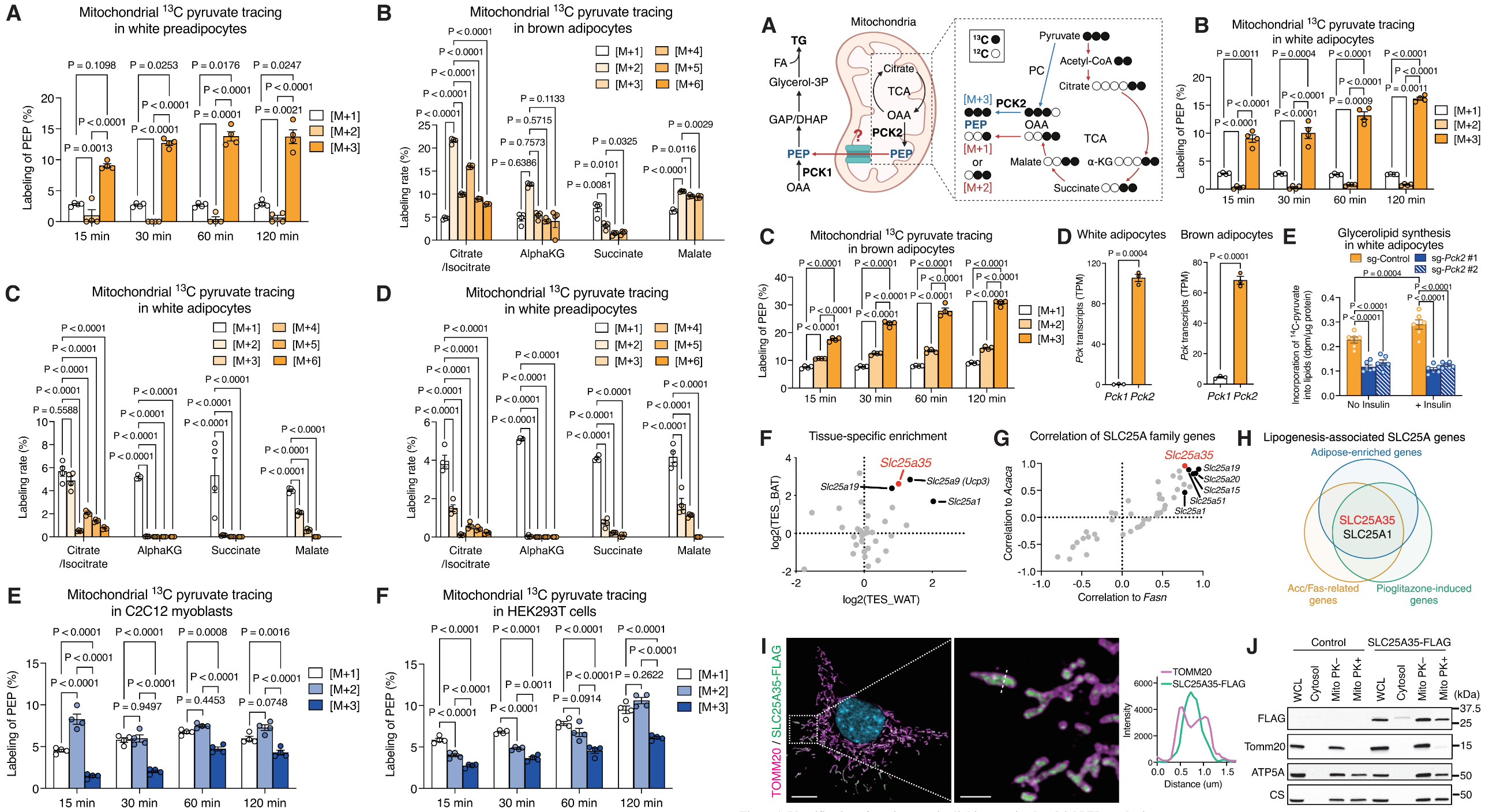
首先,作者通过同位素示踪实验证实,在白色与棕色脂肪细胞的线粒体中,13C3-丙酮酸主要代谢生成M+3标记的磷酸烯醇式丙酮酸(PEP);这一结果表明,经丙酮酸→草酰乙酸→PEP 的 “丙酮酸-PEP 旁路”,是脂肪细胞线粒体合成 PEP 的核心途径,且该过程存在显著的细胞类型选择性。线粒体基质内生成的PEP,是如何跨越线粒体内膜转运至胞质的?线粒体型磷酸烯醇式丙酮酸羧激酶(PCK2)是脂肪细胞中PEP合成的关键主导酶,PCK2敲除会显著损伤脂肪细胞的甘油酯合成能力,线粒体中可能存在尚未被鉴定的PEP输出载体。
为鉴定该候选载体,研究团队采用了三个策略进行筛选:①可高效生成M+3标记PEP的白色、棕色脂肪细胞中高表达的线粒体载体基因;②与脂肪合成关键酶编码基因Acaca、Fasn的表达水平呈显著正相关的载体基因;③被脂肪生成刺激剂(如 PPARγ 激动剂)诱导表达的载体基因。SLC25A35与已知的柠檬酸载体SLC25A1共同被锁定为候选靶蛋白。进一步分析显示,SLC25A35在脂肪组织中高表达,且与高脂质合成能力的脂肪细胞亚群共定位。最后,通过高分辨率显微镜和蛋白水解酶保护实验,证实SLC25A35蛋白特异性定位于线粒体内膜,这为其作为PEP输出载体的功能提供了关键的细胞定位基础。
2. SLC25A35是线粒体PEP外流的必需蛋白
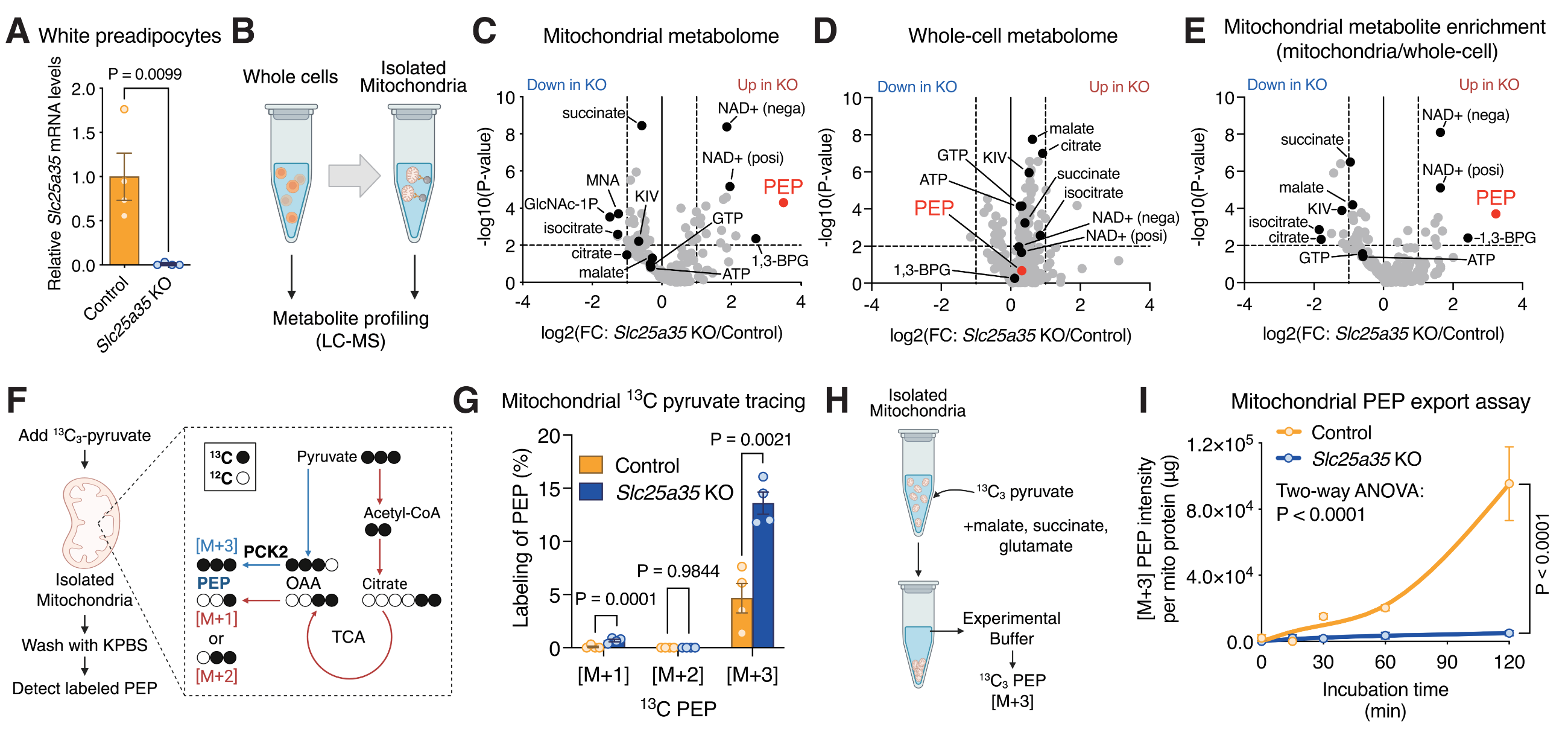
作者通过敲除SLC25A35的脂肪前体细胞,其分离线粒体中PEP、NAD+和1,3-二磷酸甘油酸等代谢物水平显著升高,而全细胞水平变化不大;计算线粒体富集度发现,PEP在线粒体内的积累最为显著(达9.4倍)。同位素示踪实验进一步显示,敲除细胞的线粒体中积累的PEP主要是由丙酮酸经丙酮酸羧化酶和PCK2新合成的PEP M+3,且其积累呈时间依赖性,而丙酮酸通过TCA循环氧化的活性未受影响。最关键的是,作者建立了一个直接测量线粒体PEP输出的实验系统,发现正常线粒体能随时间主动向培养基中分泌13C标记的PEP,而敲除SLC25A35的线粒体此分泌能力大幅下降。这些数据共同表明,SLC25A35的缺失导致由PCK2在线粒体内新合成的PEP因无法输出而积累,从而直接证明了SLC25A35介导了线粒体PEF的主动外排。
3. SLC25A35介导的PEP转运功能重构
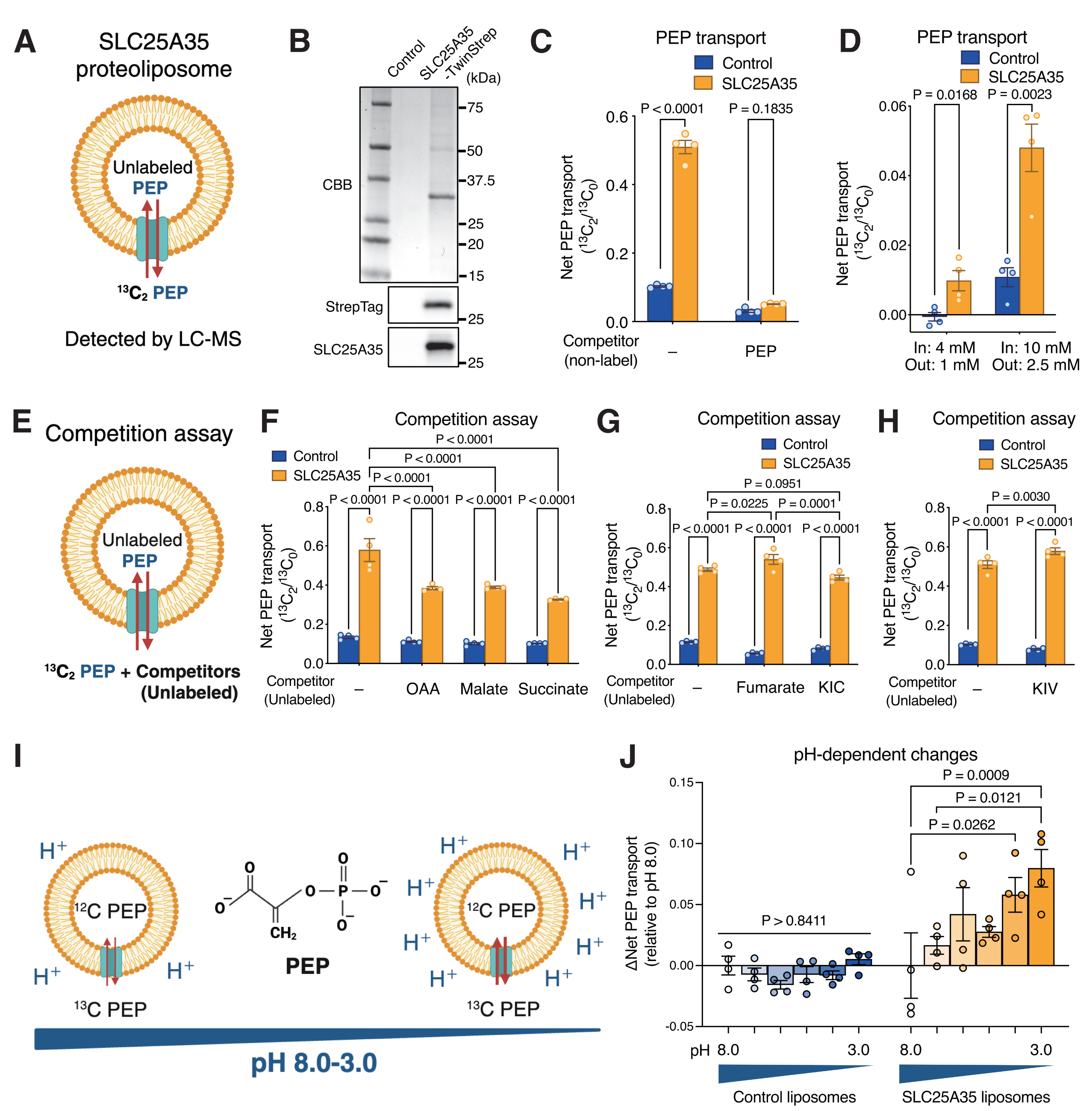
作者利用杆状病毒系统表达并纯化了小鼠SLC25A35-TwinStrep融合蛋白,并将其成功插入脂质体膜中。实验结果表明在预载未标记PEP的SLC25A35脂质体中,13C标记PEP的转运活性显著高于空载体对照组,且该转运可被过量未标记PEP完全抑制,证实了SLC25A35对PEP的特异性转运。进一步的底物竞争实验揭示,除PEP外,草酰乙酸(OAA)、苹果酸和琥珀酸也能部分抑制13C-PEP的转运,提示这些三羧酸循环中间产物可能是SLC25A35的潜在低亲和力底物;而富马酸、α-酮异戊酸(KIV)和α-酮异己酸(KIC)则无竞争效应。
值得注意的是,在酸性pH条件下(模拟高线粒体膜电位状态),SLC25A35介导的PEP转运活性显著增强。这一结果提示,线粒体内膜两侧的质子梯度(即膜电位)可能是驱动SLC25A35进行PEP逆向转运的重要能量来源。
4. SLC25A35介导PEP转运的结构机制解析
利用AlphaFold预测的人源SLC25A35结构显示其具有溶质载体典型的六次跨膜通道,腔内富含保守的极性/碱性氨基酸。分子对接与动力学模拟表明,PEP能稳定结合于该空腔,其磷酸基团与Q73、R276形成氢键/盐桥,羧酸基团与R175、Y124、Y72相互作用,结合自由能为-26.58 kcal/mol。功能实验发现,单点突变体Y124A和R175A的PEP转运活性与野生型相似,而双突变体Y124A/R175A和三突变体Y124A/R175A/R276A的转运活性反而更高,这可能类似于其他SLC25载体中“盐桥网络削弱导致门控泄漏”的机制。这些结果共同证实了Y124、R175和R276是SLC25A35介导PEP转运的关键功能残基。
5. SLC25A35介导的PEP转运是脂肪组织甘油异生的必需环节
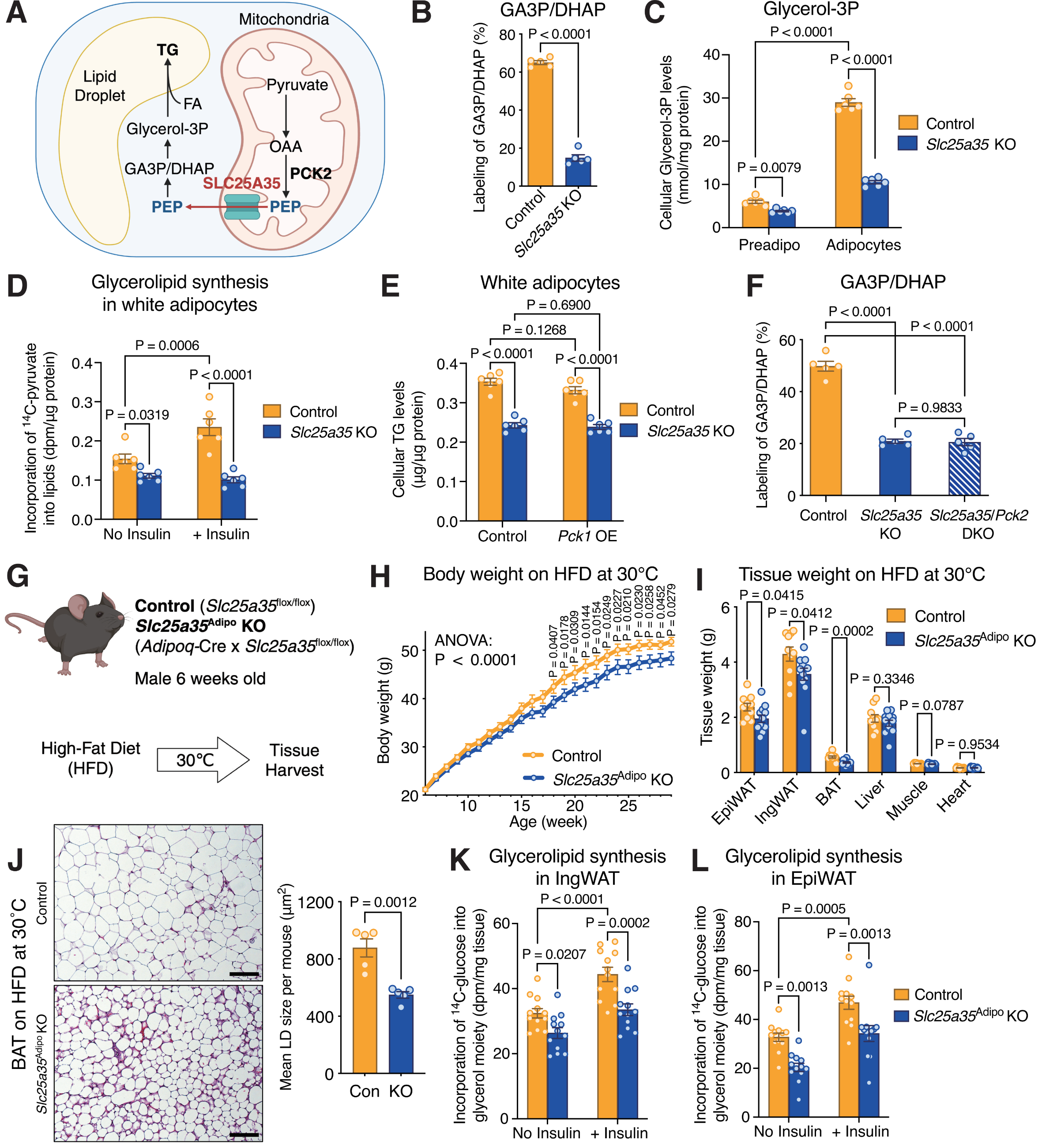
在脂肪细胞中,Slc25a35敲除会使13C3-丙酮酸示踪的13C标记GA3P/DHAP水平显著降低 77.2%,同时显著下调分化脂肪细胞与前脂肪细胞中的G3P含量。Slc25a35敲除的脂肪细胞在基础状态和胰岛素刺激条件下,同位素向脂质的掺入量均较对照细胞显著下降,细胞总甘油三酯含量也降低31.2%,且PCK1过表达无法回补该甘油三酯下降表型,Slc25a35与Pck2双敲实验进一步证实,敲除Slc25a35引发的甘油异生减弱,依赖于PCK2介导的线粒体源PEP合成,而非细胞总PEP池的变化;在此基础上构建的脂肪组织特异性Slc25a35敲除小鼠,在热中性环境高脂饮食喂养下,雄性小鼠18周龄后体重增长显著放缓,该差异源于腹股沟、附睾白色脂肪及肩胛间棕色脂肪的组织重量降低、脂肪细胞体积减小,且该表型与全身能量消耗、摄食、自主活动、脂肪组织脂解及葡萄糖氧化均无关联,同时小鼠脂肪组织中14C葡萄糖向甘油酯甘油骨架的掺入量显著降低,而向脂肪酸部分的掺入无显著差异。研究明确了 SLC25A35通过介导线粒体PEP的胞质输出,支撑脂肪组织的甘油异生过程,为甘油酯合成提供必需的甘油骨架G3P,是脂肪组织甘油酯合成的关键调控机制。
6. 阻断线粒体PEP外流可改善肝脂肪变性
通过构建肝脏特异性敲除(Slc25a35Liver KO)或使用腺相关病毒(AAV)诱导性敲除SLC25A35,作者发现,阻断该通路能显著减轻小鼠肝脏的脂肪变性:肝脏重量、甘油三酯含量、脂滴面积以及包括甘油三酯、二酰甘油、磷脂在内的多种脂质物种均显著减少,同时伴随血清和肝脏中甘油水平下降。这种脂质堆积的缓解还带来了代谢益处的连锁反应——肝脏巨噬细胞浸润和炎症基因表达减少,全身胰岛素敏感性提高,肝脏损伤标志物(ALT/AST)水平下降。重要的是,原代肝细胞实验表明,SLC25A35缺失并不影响糖异生,说明其作用特异于甘油酯合成通路。综上所述,靶向SLC25A35介导的线粒体PEP输出,能够选择性地抑制肝脏病理性脂质合成,从而缓解脂肪肝及其相关的炎症和胰岛素抵抗,展现出潜在的治疗前景。
03 研究结论
1.鉴定关键转运蛋白
首次发现并证实SLC25A35是线粒体内膜上负责将PEP从线粒体基质转运到细胞质的特异性载体蛋白。它通过依赖线粒体膜电位(质子梯度)的方式主动输出PEP,像一个受能量状态调控的“分子阀门”。
2.揭示全新代谢通路
阐明了“线粒体PEP穿梭”机制:在线粒体内,丙酮酸通过PCK2途径生成PEP,然后由SLC25A35运出,为胞质中的甘油异生提供关键的甘油骨架前体。
3.确立重要治疗靶点
SLC25A35在肥胖和脂肪肝状态下表达上调。通过基因敲除或抑制其功能,可以选择性减少甘油三酯合成,有效缓解甚至逆转肝脏脂肪变性,同时改善全身胰岛素抵抗,且不损害肝脏的基础代谢功能或引发明显毒性。这使其成为治疗代谢相关脂肪性肝病(MASLD)和2型糖尿病的极具潜力的全新药物靶点。
该研究解开了一个长期未明确的代谢谜题,不仅重新定义了线粒体在脂质合成中的主动角色,还为代谢性疾病的精准治疗开辟了全新的方向。




