Gut:浙大团队揭示胰腺癌肝转移关键蛋白,驱动线粒体重编程为肿瘤供能
01 文章导读
肝转移是胰腺导管腺癌(PDAC)患者常见且致命的并发症,其中肝脏是 PDAC 患者最主要的转移部位,即便接受原发灶根治性切除术的患者,仍有约56%会出现肝转移复发。
在转移过程中,肿瘤细胞通过代谢重编程以应对靶器官微环境中有限的营养供给,从而维持其高能量需求。线粒体动态失调不仅会重塑细胞代谢模式,还可能影响免疫细胞功能,进而促进免疫抑制性肿瘤微环境(TME)的形成与转移进展。然而,PDAC肝转移过程中驱动线粒体功能重编程的关键分子及其在塑造免疫抑制微环境中的具体机制尚不明确。近期,《Gut》期刊发表了一项题为“MTFP1 drives pancreatic cancer liver metastatic colonisation by regulating mitochondrial metabolism reprogramming”的研究文章。
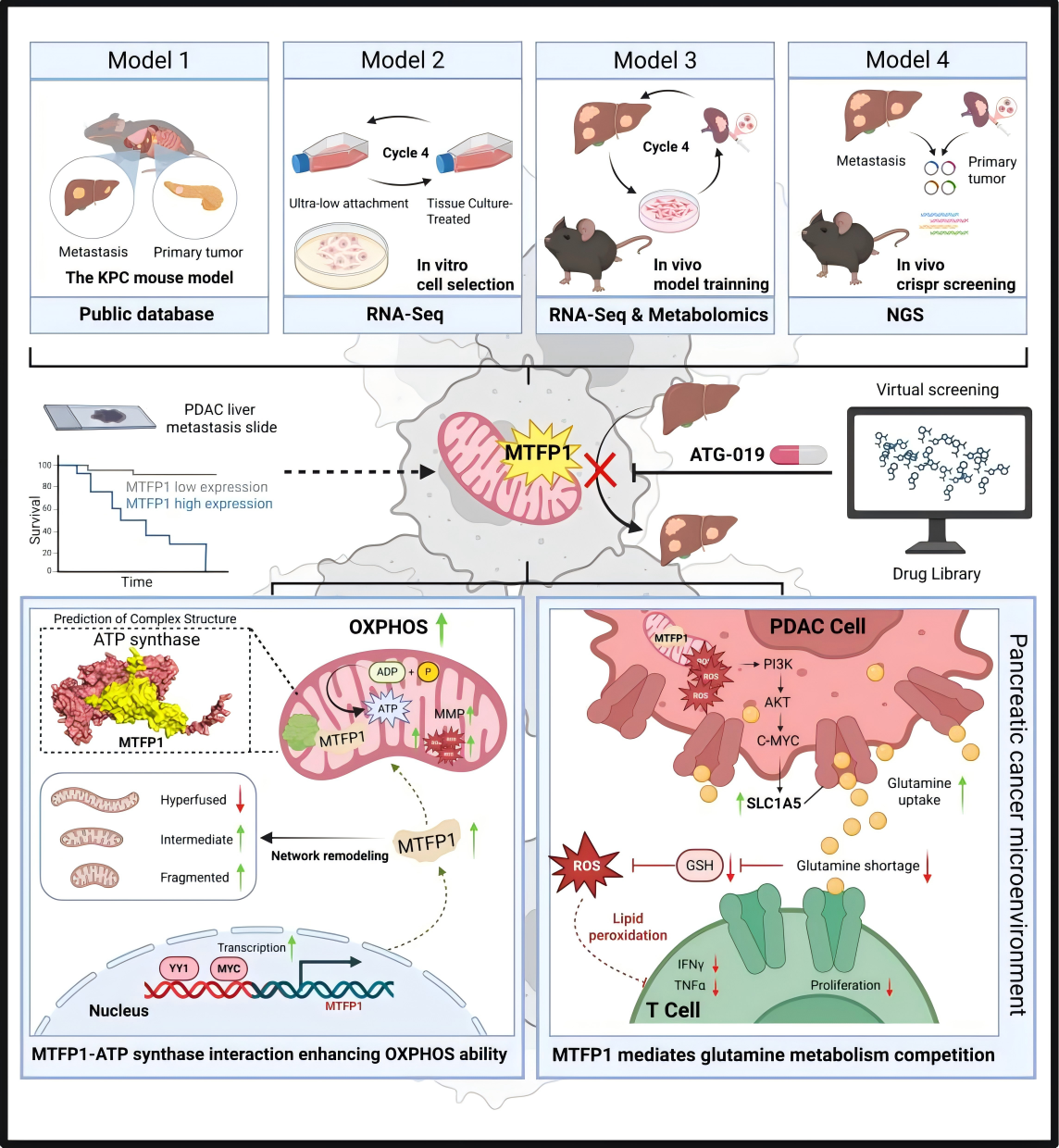
该研究通过体内外克隆筛选技术构建了具有增强肝转移能力的 PDAC 细胞系,揭示了线粒体分裂过程蛋白1(MTFP1)是 PDAC 肝转移的关键调控因子,并证实其通过重塑线粒体网络和重编程线粒体谷氨酰胺代谢发挥作用。

谱领生物提供谷氨酰胺代谢流检测技术服务
02 研究内容及结果
1. 基于CRISPR抑制与体内筛选策略建立胰腺癌肝转移小鼠模型
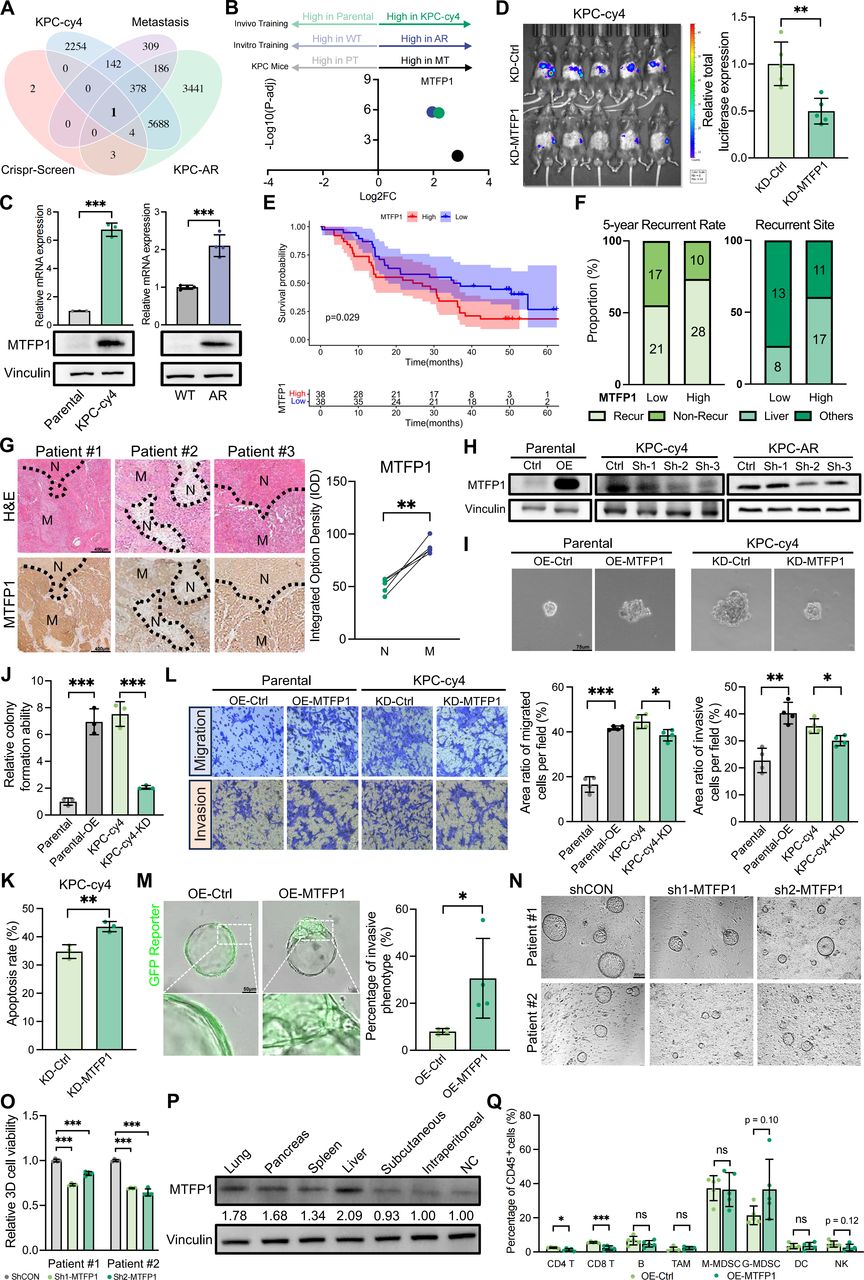
作者利用CRISPRi筛选结合MAGeCK算法分析不仅揭示了FOCAD和HBP1等富集的抑转移基因,还发现KCNF1、MECP2和MTFP1等显著耗减、在肝定植中功能未知的潜在促转移基因。随后通过四轮体内选择获得高肝转移潜能的KPC-cy4亚系,并通过失巢凋亡抵抗筛选建立KPC-AR细胞系,两者均表现出增强的肝转移能力、增殖存活优势及上皮-间质转化(EMT)特征。进一步研究发现,这些高转移细胞系不仅具有更高的基因组不稳定性和伪足形成能力,还能重塑免疫微环境(T细胞和NK细胞减少,髓源性抑制细胞增多),为解析PDAC肝转移机制提供了重要模型。
2. MTFP1驱动PDAC在肝脏的定植
通过比较体内CRISPRi筛选的前10个高表达基因、RNA测序数据以及自发性 PDAC 肝转移的公开RNA测序数据集发现mitochondrial fission process 1(MTFP1)被鉴定为驱动胰腺导管腺癌(PDAC)肝定植的关键分子,其高表达与患者总生存期缩短、复发率升高(尤其以肝复发为主)及肿瘤细胞基因组不稳定性增加密切相关。功能上,MTFP1通过增强PDAC细胞在应激条件下的增殖、存活、抗凋亡、克隆形成及迁移侵袭能力,促进肿瘤细胞的内在适应性;体内实验证实敲低MTFP1可显著抑制肝转移,而过表达则促进肝定植,且该作用不依赖于原发肿瘤生长,但在免疫健全小鼠中更为显著,伴随肝转移微环境中CD4+ T和CD8+ T细胞浸润减少,提示MTFP1通过增强肿瘤细胞自身适应性和重塑免疫微环境双重机制驱动PDAC肝转移。
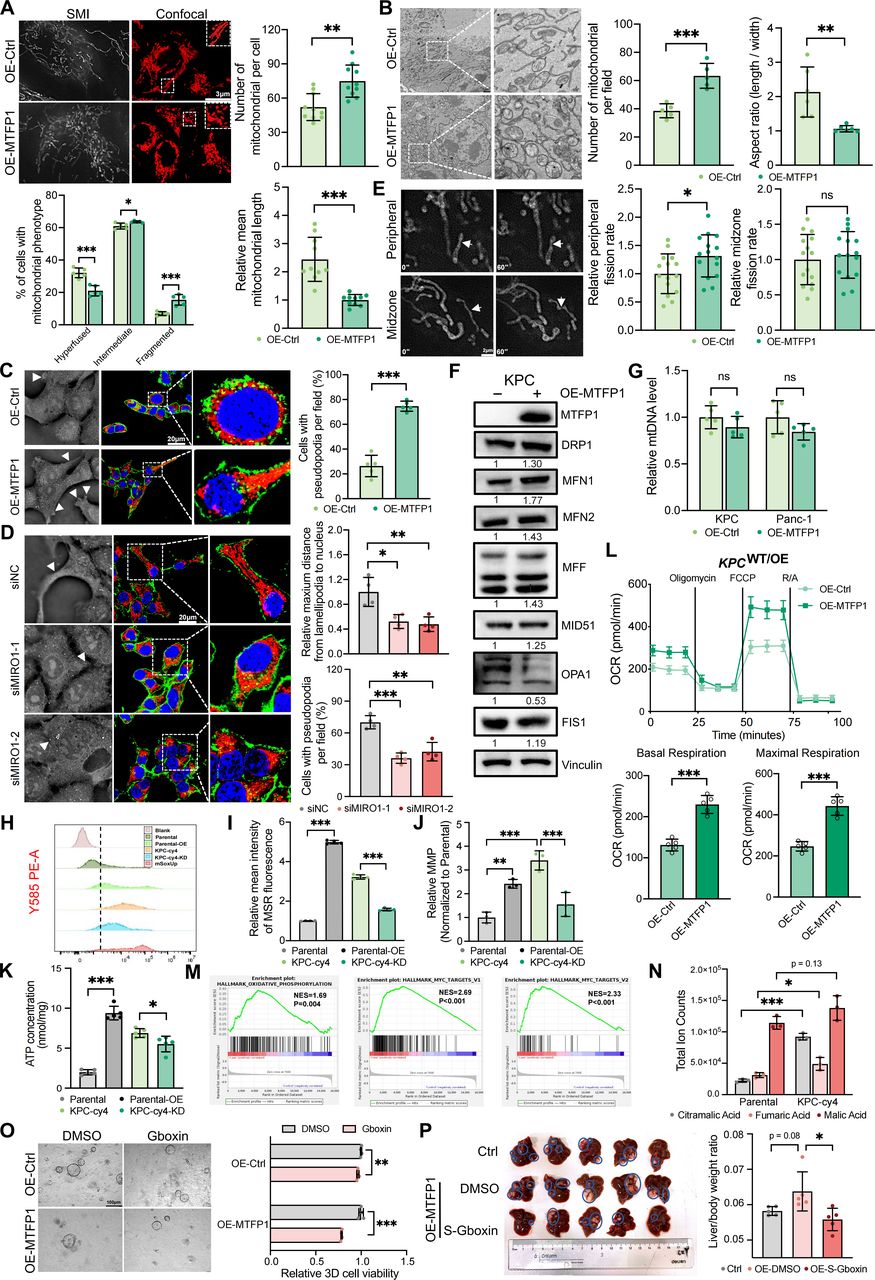
3. MTFP1通过重构线粒体形态与功能驱动PDAC肝定植
MTFP1过表达诱导线粒体碎片化(过度融合减少,中间态和碎片化比例增加),并促使线粒体借助mitochondrial Rho GTPase-1 (MIRO1)从核周向细胞前沿伪足区域重新分布,为局部侵袭提供能量。活细胞成像显示,MTFP1过表达选择性增加线粒体外周分裂和瞬时融合事件,同时下调内膜融合蛋白optic atrophy 1(OPA1),但不改变线粒体DNA含量,提示其重塑的是既有线粒体网络的分布与动态而非总量。
此外研究表明MTFP1过表达显著提升线粒体活性氧、膜电位和ATP生成,Seahorse分析证实ATP增加源于耗氧率提升,表明氧化磷酸化增强。在高转移潜能的KPC-cy4和KPC-AR细胞中同样观察到线粒体质量增加、氧化磷酸化及TCA循环通路富集。氧化磷酸化抑制剂Gboxin可逆转MTFP1过表达所加剧的肝定植,且MTFP1过表达类器官对Gboxin更敏感。综上,MTFP1通过重构线粒体网络并增强氧化磷酸化,给予肿瘤细胞在肝脏微环境中定植所需的能量支持。
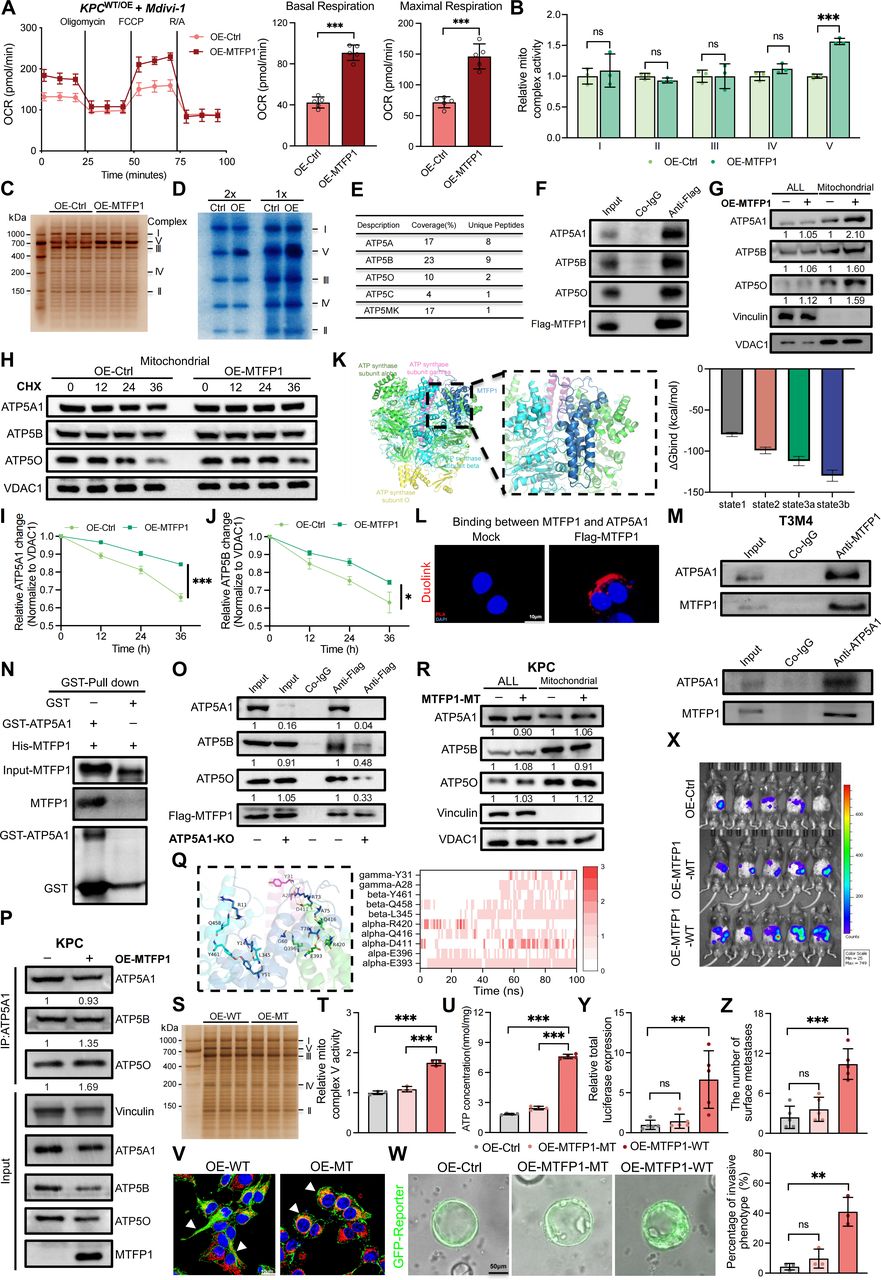
4. MTFP1直接结合ATP合酶亚基
MTFP1过表达不依赖线粒体数量增加(线粒体分裂抑制剂(Mdivi-1)处理后氧化磷酸化差异仍存在),而是特异性增强复合物V(ATP合酶)活性,对复合物I–IV无显著影响。Co-IP联合质谱鉴定发现MTFP1与ATP合酶亚基ATP5A1、ATP5B、ATP5O直接结合,且MTFP1虽不影响其总蛋白及mRNA水平,但显著延缓其在线粒体内的降解,促进线粒体积累。分子动力学模拟及突变验证显示,MTFP1通过R73/T78残基与ATP5A1的E393、E396等位点形成稳定氢键,以ATP5A1为核心锚点,进而增强ATP5A与ATP5O亚基间互作,促进合酶组装。破坏此结合(R73A/T78A突变)可消除MTFP1对ATP合酶活性、线粒体积累及ATP生成的增强作用,并逆转了野生型MTFP1在小鼠体内加速的肝转移进程。综上,MTFP1通过直接结合并稳定ATP合酶核心亚基(尤其是ATP5A1),增强合酶组装与线粒体积累,提升氧化磷酸化活性,增强PDAC的肝脏定值能力。
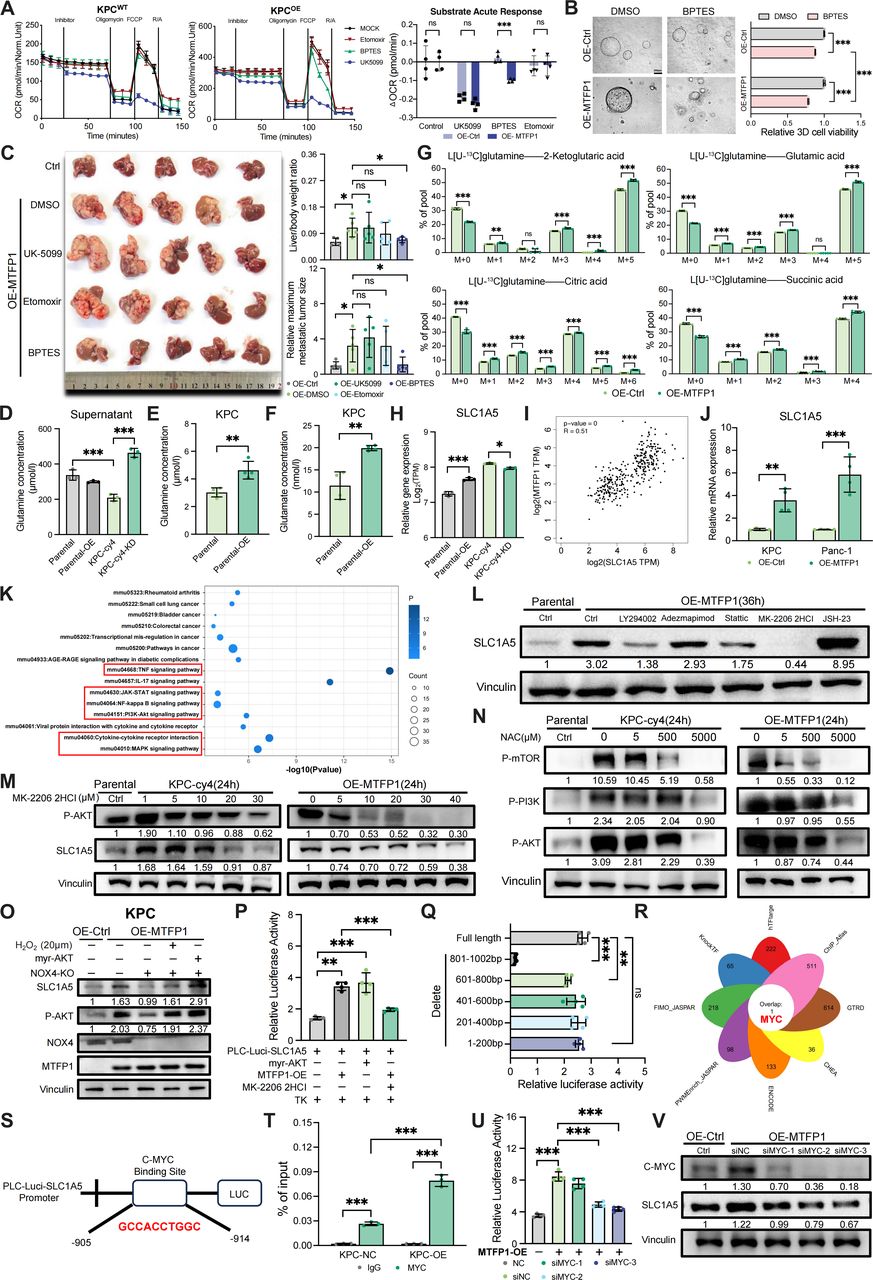
5. MTFP1通过ROS-PI3K-AKT-c-MYC通路上调SLC1A5增强谷氨酰胺驱动的氧化磷酸化能力
MTFP1过表达使细胞对谷氨酰胺酶抑制剂BPTES更敏感,体内BPTES处理可显著抑制肝转移负荷;为直接验证MTFP1对谷氨酰胺摄取的调控作用,作者检测了PDAC细胞的谷氨酰胺摄取量,发现MTFP1过表达显著提升了细胞内谷氨酰胺和谷氨酸水平,并在富含谷氨酰胺的培养基中大幅增强了谷氨酰胺摄取。进一步基于[U-13C]-glutamine的代谢流分析揭示了MTFP1过表达加速谷氨酰胺消耗,增加谷氨酸及TCA循环中间产物(如α-酮戊二酸、柠檬酸、琥珀酸)的富集,表明谷氨酰胺进入TCA循环为氧化磷酸化提供底物。
基于RNA-seq数据发现谷氨酰胺转运体SLC1A5与MTFP1表达呈正相关。过表达MTFP1可同时上调SLC1A5的mRNA和蛋白水平,该作用主要通过PI3K-AKT信号通路实现。使用ROS清除剂NAC或敲除NOX4可阻断MTFP1引起的PI3K-AKT激活及SLC1A5上调,而外源性H₂O₂或组成型激活的myr-AKT能逆转该抑制效应。MTFP1通过AKT激活转录因子c-MYC,c-MYC直接结合SLC1A5启动子区-905bp至-914bp位点,促进其转录。此外,MTFP1自身的表达受转录因子YY1和c-MYC共同调控,二者可直接结合其启动子区。PDAC单细胞数据分析显示,MTFP1与YY1的表达随肿瘤细胞从原发灶向转移进展呈上升趋势,提示其在胰腺癌转移中具有潜在作用。
6. MTFP1介导的肿瘤细胞与T细胞间谷氨酰胺代谢竞争
单细胞测序和流式细胞术显示MTFP1过表达的肿瘤微环境中CD8⁺T细胞比例减少、功能受损,且与肿瘤细胞MTFP1表达水平呈负相关;CD8⁺T细胞耗竭可逆转MTFP1过表达所致的肝定植增强,证实T细胞是关键效应细胞。排除经典免疫抑制机制后,研究发现MTFP1通过上调SLC1A5增强肿瘤细胞谷氨酰胺摄取,导致微环境中谷氨酰胺匮乏,共培养体系中T细胞增殖与杀伤功能受抑。体内实验证实,SLC1A5敲除可消除MTFP1过表达对肝转移的促进作用。深入机制表明,谷氨酰胺竞争导致CD8⁺T细胞内谷胱甘肽合成受阻,引发线粒体活性氧累积、脂质过氧化增强,单细胞轨迹分析显示T细胞从效应向耗竭状态转化,且氧化应激与铁死亡通路活化;谷氨酰胺补充或铁死亡抑制剂Ferrostatin-1可挽救T细胞死亡,而凋亡或坏死抑制剂无效。人源样本验证显示,肝转移灶中谷氨酰胺富集区域呈现Ki-67⁺肿瘤细胞增多而CD8⁺ T细胞减少的特征。综上,MTFP1通过SLC1A5介导的谷氨酰胺摄取增强,剥夺CD8⁺ T细胞的谷氨酰胺供应,抑制其谷胱甘肽合成并诱发氧化损伤与铁死亡,导致T细胞耗竭,从而实现免疫逃逸并促进PDAC肝定植。
7. KPT 9274 (ATG-019)直接结合MTFP1并抑制PDAC肝转移
通过药物重筛选发现KPT 9274可直接结合MTFP1并抑制PDAC肝转移。研究从34735种化合物中筛选出KPT 9274,体内验证其可显著抑制肝转移、延长生存期且无明显毒性。SPR证实其与MTFP1直接结合,分子动力学模拟显示复合物结构稳定。KPT 9274可消除MTFP1过表达所致的ATP上调,并与抗PD-L1抗体协同增效。综上,KPT 9274作为靶向MTFP1的候选化合物,为PDAC肝转移防治提供新策略。
03 研究结论
1. MTFP1 在胰腺导管腺癌(PDAC)肝转移定植过程中表达上调,且与患者不良预后相关。
2. MTFP1 介导线粒体网络发生质性的重塑,有利于生物能量代谢能力的高效分配,并增强PDAC细胞的转移表型。
3. MTFP1 通过与多个ATP合成酶亚基直接相互作用,促进ATP合成酶的组装并增强其酶活性,从而提高肿瘤细胞内在的氧化磷酸化能力。
4. 谷氨酰胺转运蛋白SLC1A5通过MTFP1/ROS/PI3K/AKT/c-MYC信号轴介导肿瘤细胞代谢竞争,从而损害抗肿瘤免疫。