Nat Metab:核纤层蛋白重塑半胱氨酸代谢,为组蛋白酰基化定向输送碳源
01 文章导读
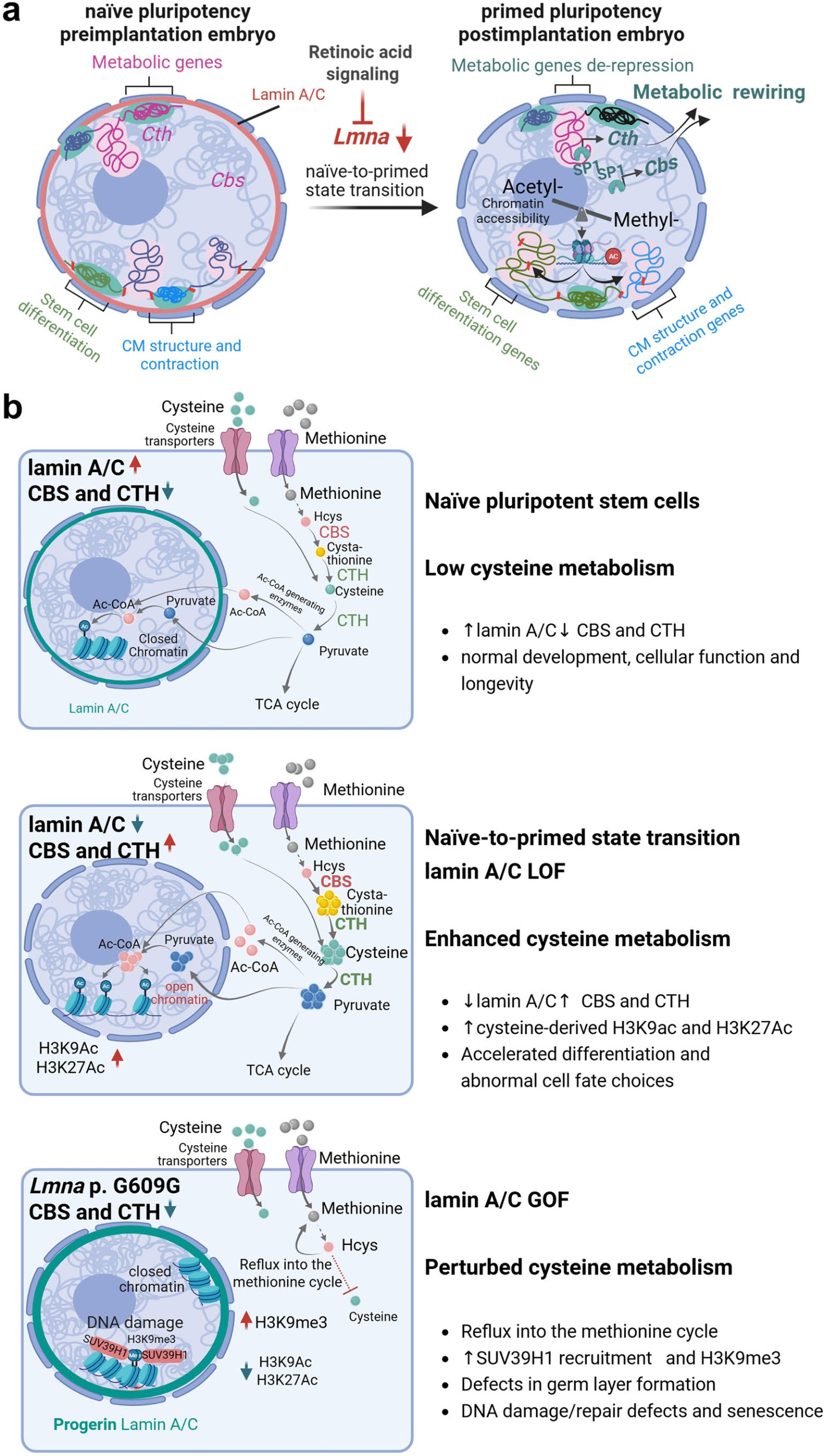
核纤层与细胞代谢的时空动态变化共同决定细胞命运,但两者之间具体的相互作用机制目前仍不清晰。已有研究提示核纤层蛋白与细胞衰老、多能性维持密切相关,而细胞代谢会通过表观修饰影响细胞状态,但核纤层如何调控代谢、代谢又如何反向影响细胞命运与衰老,这一关键链条尚未被阐明。2026年1月28日,来自海德堡大学Gergana Dobreva、Sofia-Iris Bibli团队在Nature metabolim上发表了题为Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming的文章,该研究揭示了核纤层蛋白A/C(Lamin A/C)在LADs(核纤层相关结构域)之外的表观遗传调控作用,其通过laminA/C介导的半胱氨酸向乙酰辅酶A的转运及组蛋白乙酰化过程,对胚层的正常形成、细胞命运决定和衰老过程具有关键作用。

02 研究内容及结果
1. LaminA/C抑制初始多能干细胞中半胱氨酸的生物合成与分解代谢
前期研究证实Lamin A/C(核纤层蛋白A/C)可维持该细胞三维染色质结构及原始多能性,Lmna敲除后,染色质开放区域相关基因超85%位于非LADs区域(与细胞核纤层相互作用的染色质区域);代谢组学检测显示,半胱氨酸与甲硫氨酸代谢通路异常最显著,其关键中间产物水平改变,而其他代谢通路未受影响。半胱氨酸代谢关键酶胱硫醚β合成酶(CBS)和胱硫醚γ裂解酶(CTH)中,CTH定位于核周及LADs区域,Lmna敲除后CTH向核内重定位;Lamin A/C可直接结合二者启动子,其缺失会显著升高CBS、CTH的染色质可及性、转录及蛋白表达水平。
另外,启动子区域基因测序分析证实转录因子SP1是调控CBS、CTH的关键因子,Lmna敲除会增强SP1在二者启动子的结合,沉默SP1可逆转其上调,而ATF4(细胞应激时被激活的关键转录因子,可调控CTH和CBS的表达水平)无明显变化;同时,Lamin A/C通过招募PRC2复合物催化H3K27me3修饰,限制SP1结合,从而抑制CBS、CTH表达。此外,Lmna p.G609G突变(该突变会产生显性功能获得性的早老素progerin,导致早老症HGPS)的影响:该突变使染色质开放区域减少,且减少的区域中超过70%位于非LADs区域;KEGG通路分析显示,突变细胞中下调的基因主要集中在一碳代谢、半胱氨酸与甲硫氨酸代谢通路,与Lmna敲除的变化趋势一致,但效应相反——Lmna突变细胞中CTH、CBS的表达量,以及细胞内半胱氨酸、丙酮酸、乙酰辅酶A的水平均显著降低,同时SP1与染色质的结合能力下降,SP1在CBS和CTH启动子区域的富集度减少,而H3K27me3修饰和Lamin A/C的富集度则显著升高。
综上,Lamin A/C功能异常(缺失或突变),会通过调控SP1结合及H3K27me3修饰,直接影响初始多能干细胞的半胱氨酸代谢。
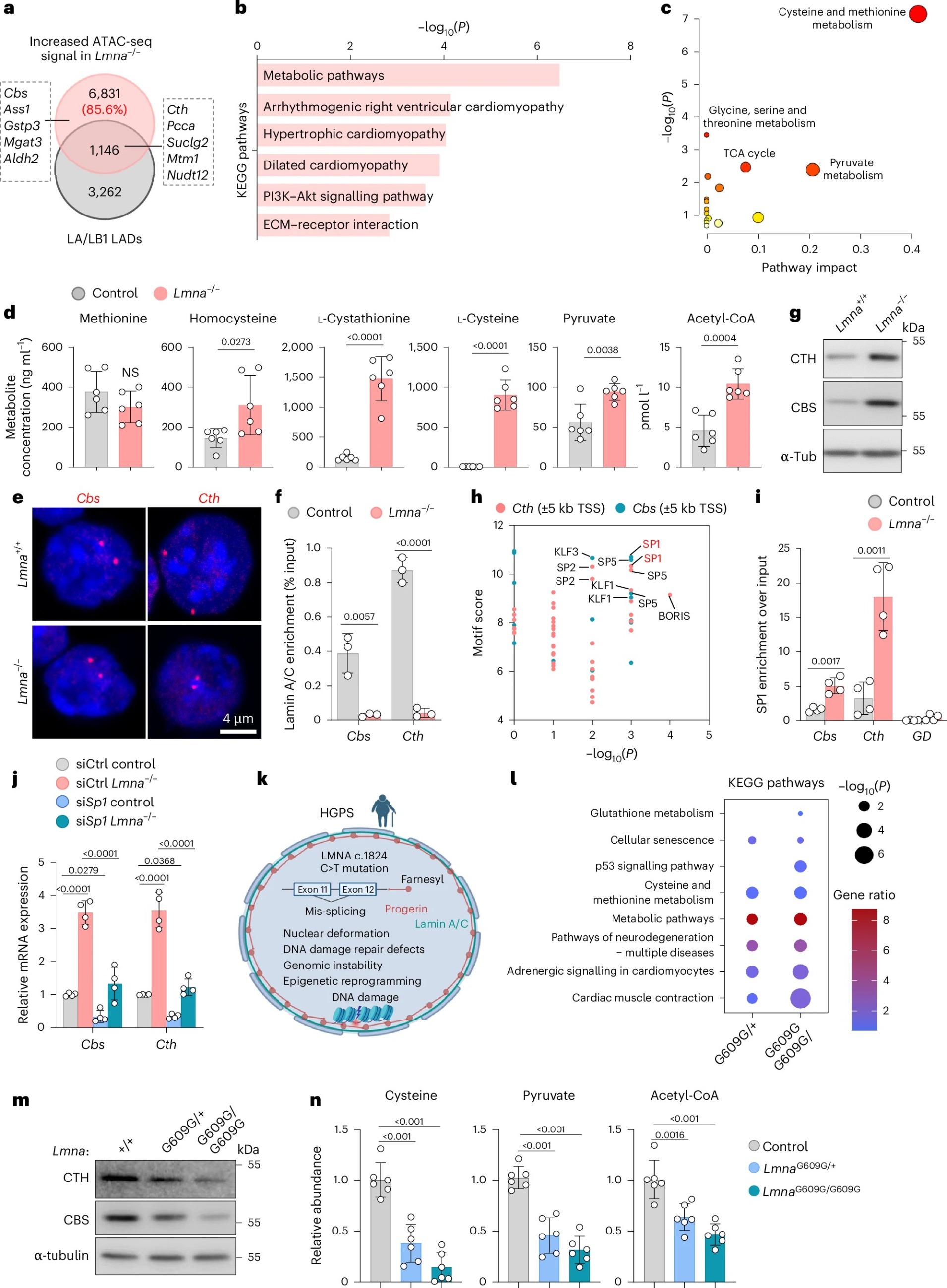
图1 LaminA/C抑制初始多能干细胞中半胱氨酸的生物合成与分解代谢
2. CTH和CBS在从naive向primed转变过程中以Lamin A/C依赖性方式上调
Lamin A/C缺失会导致小鼠胚胎干细胞(mES细胞)从初始多能态(naive态)向启动多能态(primed态)转换,并引发发育过程中异常的细胞命运选择。为进一步探究核纤层-半胱氨酸分解代谢轴对干细胞分化的影响,代谢组学分析显示,甲硫氨酸代谢和同型半胱氨酸降解是干细胞向三胚层分化过程中富集最显著的通路之一,且与naive态mES细胞相比,第3天类胚体(EB)中同型半胱氨酸、胱硫醚和半胱氨酸水平显著升高,其中胱硫醚和半胱氨酸水平在后续阶段仍维持在高位,提示半胱氨酸代谢在干细胞分化早期发挥重要作用。将naive态mES细胞诱导为primed态后,核纤层蛋白A/C表达降低,同时CTH和CBS的表达显著上调,细胞内半胱氨酸水平也随之升高,人胚胎干细胞(hES细胞)在naive态与primed态培养条件下也呈现类似结果。
功能验证显示,敲低Lmna−/− mES细胞中的Cth或Cbs基因,可使其集落形态恢复为naive态细胞特有的致密圆形,并增加高表达多能性标志物OCT4和NANOG的细胞数量;而过表达CTH或CBS则会促使mES细胞形成扁平不规则集落,且OCT4high和NANOGhigh细胞数量减少,同时敲低Cth或Cbs还可降低Lmna−/− mES细胞中primed态标志物的表达(其中Cth敲低效果更显著)。此外,半胱氨酸耗竭(单独使用或与CTH、CBS抑制剂AOAA联合使用)可增加OCT4high和NANOGhigh mES细胞的数量。利用TET-ON诱导系统在野生型和Lmna−/− mES细胞中过表达核纤层蛋白A-绿色荧光蛋白(GFP),发现核纤层蛋白A表达升高会显著降低CTH、CBS的表达及细胞内半胱氨酸水平,且即使在primed态培养条件下,也能促进naive态特征的获得;在R1 mES细胞(129X1×129S1品系的F1杂交体)中消融了Lmna后,同样观察到CTH、CBS表达及半胱氨酸水平升高,细胞向primed态转换的现象。综上,这些结果表明,CTH和CBS的上调是干细胞从naive态向primed态转换的保守特征,且该过程依赖于Lamin A/C的调控。

图2 CTH和CBS在从naive向primed转变过程中以Lamin A/C依赖性方式上调
3. 植入前-植入后转变伴随Lamin A/C表达下降与CTH/CBS水平升高
植入前(E3.5、E4.5,初始多能性)至植入后(E5.5–E6.75,启动多能性),小鼠胚胎中Lamin A/C表达下降,Cth、Cbs水平升高。scRNA-seq及免疫染色显示,Lmna在植入前早期上胚层高表达,Cth、Cbs低表达;E5.5起,Lmna急剧下调,二者显著升高。为探究Lmna下调机制,TOBIAS足迹分析显示,视黄酸(RA)信号受体RARA:RXRG、RARB是其首要候选调控因子。RA处理mES细胞后,Lmna 与Nanog的表达均显著下调,提示RA信号在多能性转变过程中介导Lmna的下调。KEGG通路分析显示,E5.5较E3.5上调基因富集于DNA复制、氧化磷酸化等通路;E5.5上调基因中SP1结合基序显著富集。
4. 半胱氨酸作为Lmna⁻/⁻ mES细胞H3K9/ K27ac的主要碳源
半胱氨酸作为牛磺酸、谷胱甘肽等重要代谢物的前体,在氧化还原平衡调控中发挥关键作用,其在Lmna⁻/⁻ mES细胞中更倾向于通过非经典分解代谢途径代谢;代谢流分析显示,Lmna⁻/⁻细胞中半胱氨酸来源的碳更倾向于流向丙酮酸与乙酰辅酶A,进而促进核内乙酰辅酶A积累,通过¹³C₃-L-半胱氨酸示踪证实,半胱氨酸是该细胞H3K9(组蛋白H3赖氨酸9)、H3K27(赖氨酸27)乙酰化的主要碳源,可特异性促进这些位点乙酰化,且该效应依赖CBS与CTH,过表达则可上调相关位点乙酰化;与之相反,Lmna p.G609G早衰点突变mES细胞中CTH/CBS表达下调,H3K9ac、H3K27ac水平显著降低,过表达CTH/CBS或提高培养基半胱氨酸浓度可部分挽救该表型;此外,Ⅰ类组蛋白去乙酰化酶(HDAC)活性并非乙酰化异常的直接原因,细胞向启动态多能性转化时CTH/CBS上调,启动态细胞及着床后胚胎中H3K9ac、H3K27ac水平更高,Lmna缺陷细胞中半胱氨酸转运体Slc1a1、Slc1a5上调但对表型的影响弱于CTH沉默,综上,核纤层调控的半胱氨酸分解代谢可在早期胚胎发育阶段动态调控组蛋白乙酰化修饰。
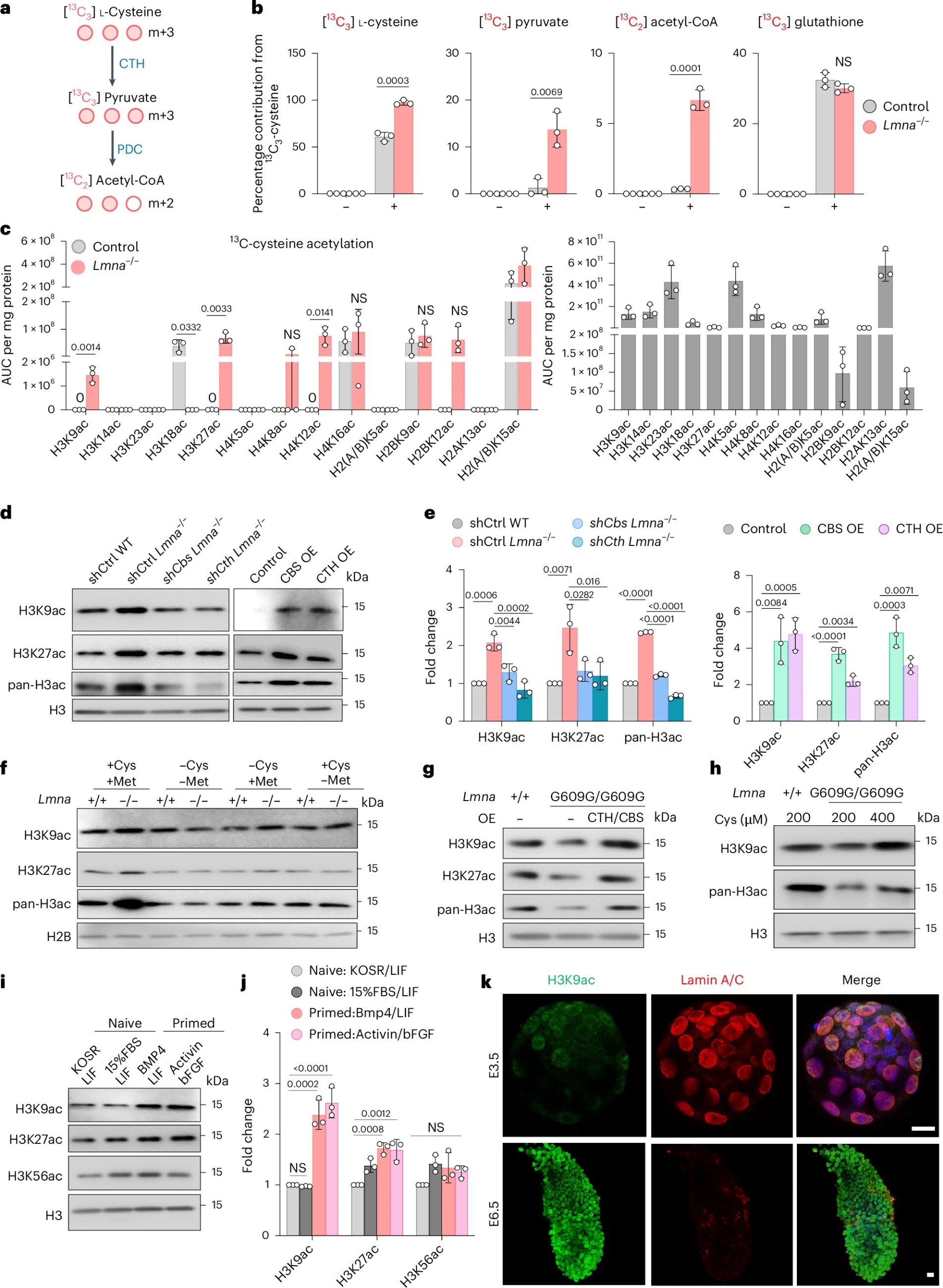
图3 半胱氨酸作为Lmna⁻/⁻ mES细胞H3K9/ K27ac的主要碳源
5. CTH激活可导致表观基因组重塑与转录激活
研究发现,在Lmna⁻/⁻ mES细胞中,染色质开放程度的变化,依赖于半胱氨酸介导的组蛋白乙酰化(H3K9ac、H3K27ac)。实验显示,这类细胞以及CTH、CBS过表达的细胞中,染色质开放程度高的区域,组蛋白乙酰化水平也更高;而染色质开放程度降低的区域,乙酰化水平也会下降。进一步研究发现,Lmna敲除后,被激活的基因会出现广泛的乙酰化升高,而部分未被激活但染色质开放的基因,仅特定区域乙酰化升高;CTH、CBS过表达只能促进被激活基因的乙酰化,沉默二者则会降低乙酰化水平,其中只有沉默CTH会影响两类基因。这说明,半胱氨酸产生的乙酰辅酶A会配合基因转录过程促进组蛋白乙酰化,而Lmna⁻/⁻是实现这一过程的必要条件。
此外,乙酰化升高还会改变细胞内非核纤层关联结构域(non-LAD)的染色质三维结构;RNA测序结果显示,Lmna⁻/⁻细胞中表达升高的基因,与沉默CTH、CBS后表达降低的基因,以及CTH、CBS过表达后表达升高的基因高度重合,且CTH和CBS会相互促进表达,它们过表达后会激活与核纤层蛋白病相关的基因。在Lmna早衰突变的细胞中,表达降低的基因,与CTH、CBS过表达后表达升高的基因也高度重合,而过表达CTH和CBS能挽救这类细胞的基因异常表达。综上,CTH和CBS在这些细胞的表观基因组结构改变和基因转录调控中,起到了关键作用。
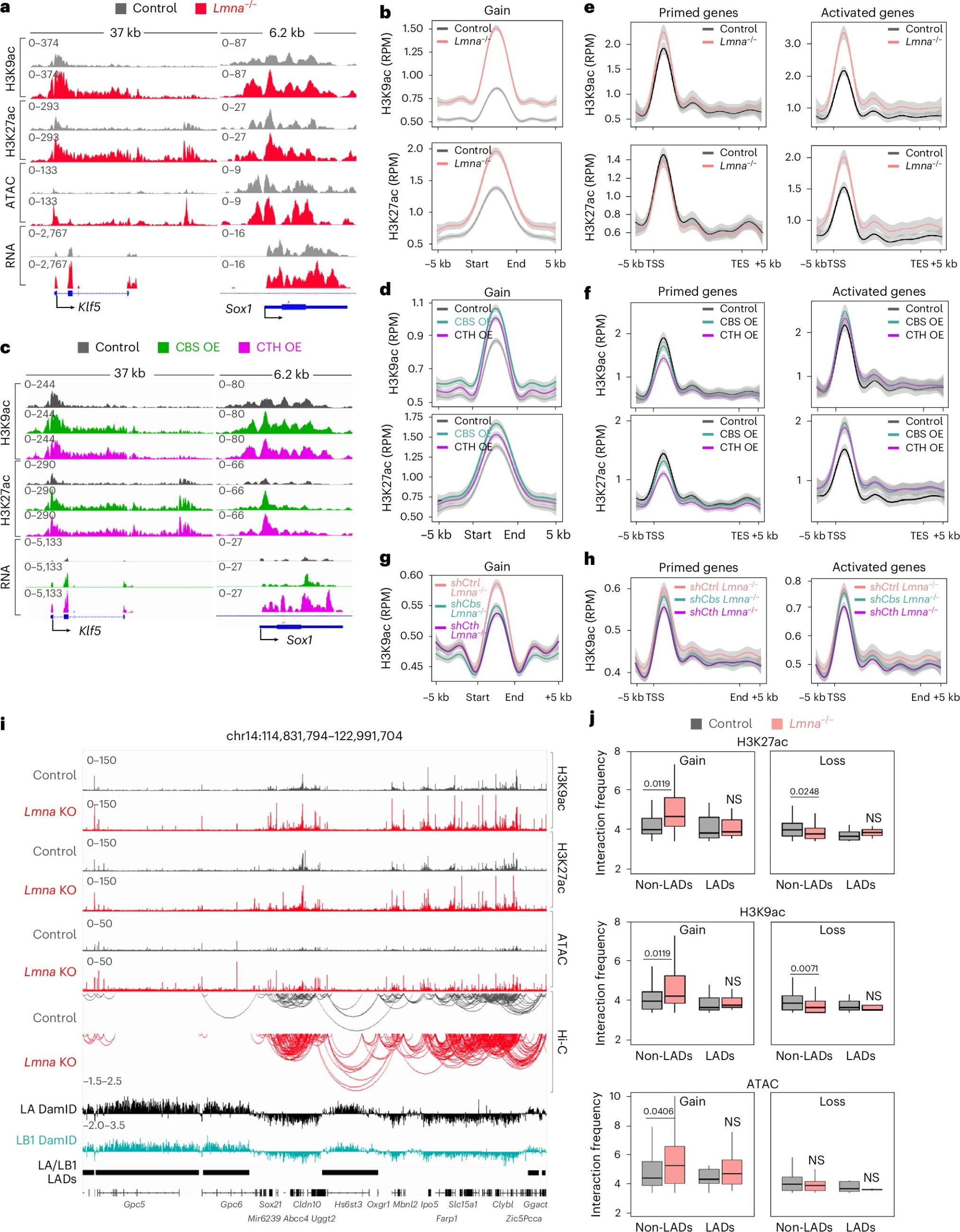
图4 CTH激活可导致表观基因组重塑与转录激活
6. CTH/CBS非生理水平表达导致细胞命运异常
Lmain A/C缺失会导致发育中细胞命运选择异常并偏向心肌细胞分化,而过表达CTH或CBS蛋白同样会促进心脏中胚层定型与心肌细胞分化,反之半胱氨酸缺乏则会抑制这一过程;沉默Cth基因可有效逆转Lmna敲除干细胞中异常增强的心肌细胞分化,沉默Cbs基因效果较弱,使用CTH/CBS抑制剂也能起到类似作用。
单细胞测序结果显示,Cth基因缺失可部分或完全挽救Lmna缺陷造成的多种细胞数量改变与转录异常;而在Lmna早衰突变细胞中,降低Cth/Cbs表达会重现胚层分化与心肌细胞分化缺陷,过表达CTH/CBS蛋白或提高培养基半胱氨酸浓度,则能挽救组蛋白乙酰化水平降低、CTH蛋白减少及心肌分化异常等表型,说明CTH和CBS通过调控半胱氨酸代谢,直接影响了Lmna突变相关的细胞命运与分化过程。
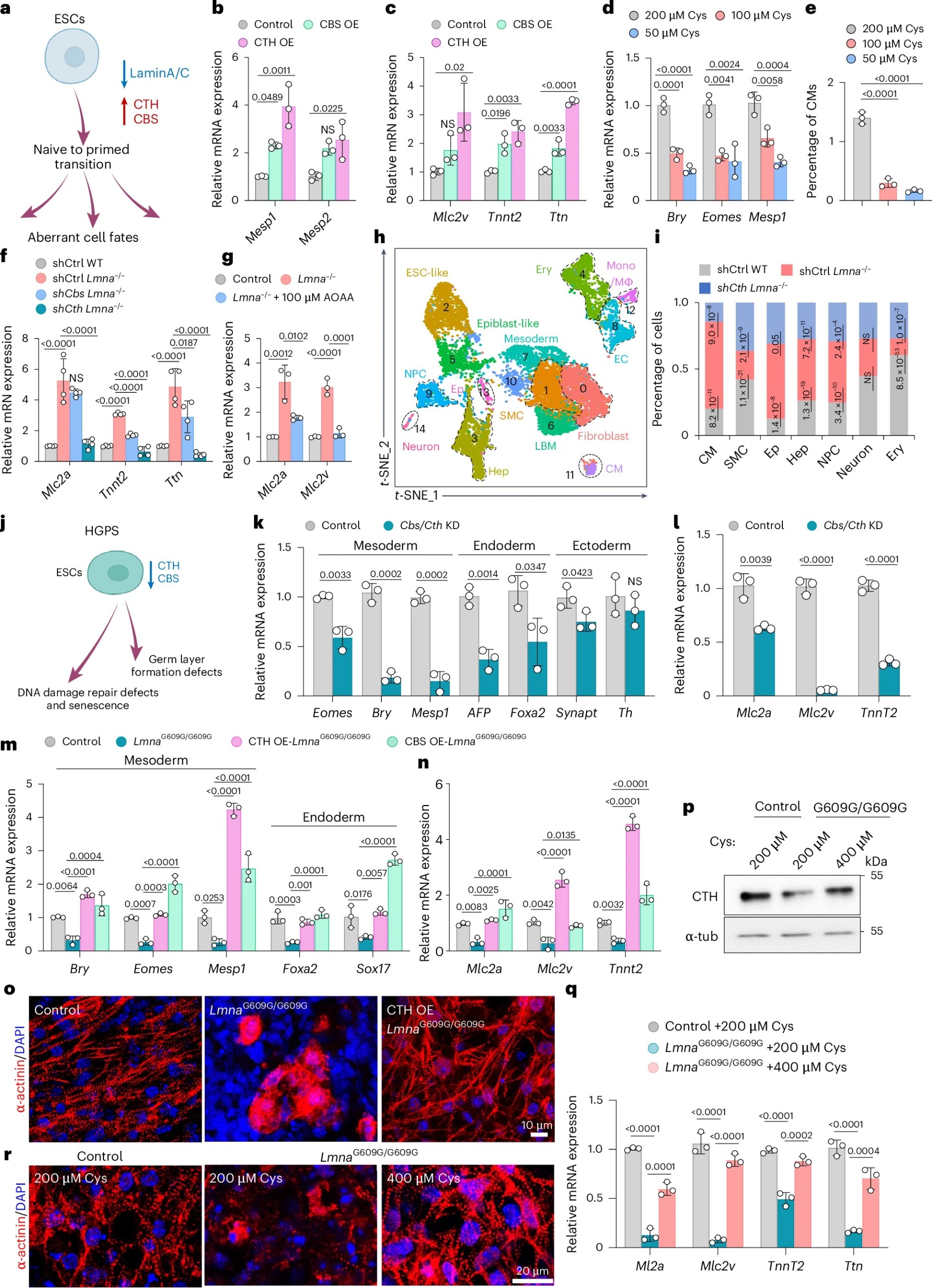
图5 CTH/CBS非生理水平表达导致细胞命运异常
7. 沉默Cth/Cbs恢复Lmna缺陷心肌细胞分化与功能
Lamin A/C缺失会造成心肌细胞过早分化、收缩节律异常、凋亡增加,并在机械应激下出现明显DNA损伤;而敲低Cth或Cbs能够改善心肌细胞过早双核化与搏动节律,减少细胞凋亡,恢复细胞增殖相关基因表达,挽救Lmna缺陷心肌细胞的多种异常表型。
8. CBS调控初始多能态干细胞H3K9甲基化-乙酰化平衡
CBS可通过调控半胱氨酸与甲硫氨酸代谢通路,改变甲基供体SAM的水平及SAM/SAH比值,进而在初始多能干细胞中平衡组蛋白H3K9的甲基化与乙酰化修饰:Lmna⁻/⁻细胞中CBS水平升高,导致SAM含量及SAM/SAH比值下降,染色质结合的SUV39H1(组蛋白甲基转移酶)减少,H3K9me3降低而H3K9ac升高;与之相反,Lmna早衰突变细胞中CBS降低,使得SAM上升、H3K9me3升高而乙酰化下降。沉默Cbs会显著提高SAM水平与SAM/SAH比值,促进SUV39H1结合染色质并增加H3K9me3,而过表达CBS则产生相反效果,且只有CBS能影响SUV39H1向染色质的招募,不改变细胞核内总SUV39H1量。综上,CBS介导的代谢流重编程通过调控SAM水平与SUV39H1的染色质结合,最终决定H3K9甲基化与乙酰化的平衡。
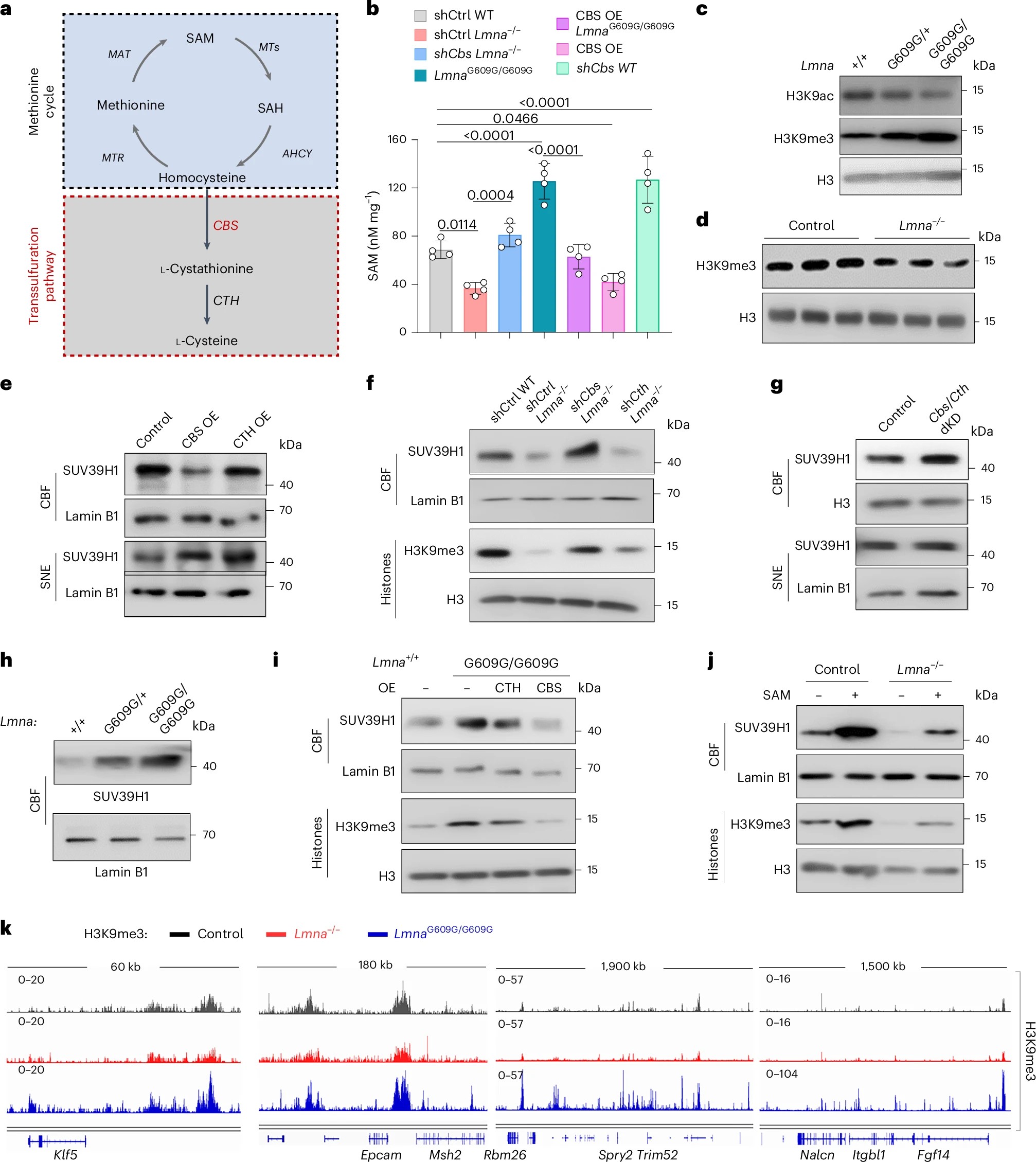
图6 CBS调控初始多能态干细胞H3K9甲基化-乙酰化平衡
9. CBS依赖性半胱氨酸代谢重编程调控 DNA损伤修复与细胞衰老
鉴于CBS水平在调控甲硫氨酸循环与半胱氨酸代谢通路代谢流中的关键作用,研究人员探究了在Lmna p.G609G mES细胞(早衰细胞)中重新表达CBS的效果,通过精准调控慢病毒滴度使CBS恢复至正常内源性水平(避免过表达诱导细胞衰老),结果显示该处理可显著减少DNA损伤(γ-H2AX染色证实,同时降低细胞衰老经典标志物SA-β-gal(SA-β-半乳糖苷酶)的活性、缓解线粒体氧化应激,并使上调的衰老相关分泌表型(SASP)基因表达回落至基线,将培养基中甲硫氨酸浓度降至10–25 µM也可得到类似效果;进一步研究发现,该机制同样参与生理性衰老与早衰症的病理过程,老年小鼠心脏中早衰蛋白(progerin)表达升高且Cbs基因水平显著下降,伴随H3K9me3升高、SASP基因上调,早衰症患者及老年人的CBS表达均低于正常水平,Lmna p.G609G小鼠SAM/SAH比值升高,而甲硫氨酸限制可降低该比值,提示早衰蛋白积累可能通过下调CBS破坏代谢平衡进而推动早衰;综上,本研究揭示核纤层蛋白A/C可通过调控一碳单位代谢流,维持正常细胞命运与功能,抑制细胞衰老和机体老化。
03 研究结论
本研究首次揭示核纤层蛋白Lamin A/C通过调控半胱氨酸代谢通量,重塑组蛋白乙酰化与甲基化平衡,进而决定干细胞命运、组织分化与衰老进程,为laminopathies(编码核纤层蛋白)及衰老相关疾病提供了代谢-表观遗传干预的新策略。