J Clin Endocr Metab丨严重Graves眼病Th1/Th17“杂合”表型与脂代谢改变的相关性证据
Greves眼病(GO)是最常见的眼眶疾病,严重的可能导致失明和致残。脂质代谢是调节Th17细胞在正常和致病条件下的关键因素,因为脂肪酸的合成可以抑制人和小鼠Th17细胞的形成并且大大促进了抗炎T细胞表型的形成,比如高血清胆固醇是GO发病的最危险因素之一,所以研究效应T细胞表型与血清脂代谢的潜在关联是非常有意义的。
2020年4月,来自上海交通大学医学院附属第九人民医院周慧芳教授及其团队在Journal of Clinical endocrinology & Metabolism在线发表了Evidence for Associations Between Th1/Th17 “Hybrid” Phenotype and Altered Lipometabolism in Very Severe Graves Orbitopathy(IF=5.49)的文章,在这项研究中作者采用流式细胞技术和脂质组学技术探究了Th1/Th17细胞系在GO患者发病机制的特征。
患者和对照组

细胞的制备和筛选
1、细胞因子谱揭示了严重Graves眼病患者Th17细胞系的可塑性
研究者通过检测患者和健康对照组中的Th1、Th17和Th17.1细胞的细胞内IFN-γ和IL-17A表达水平,发现在严重的GO患者、中重度GO患者和GD患者中观察到产生IFN-γ的Th1细胞的比例显著增加,而且Th1细胞也更丰富。但是在GO患者总的Th1细胞产生的频率最低,与其他组相比,本组产生IFN-γ的Th1细胞的比例最高。与健康对照组相比,重度GO患者、中重度GO患者和GD患者产生IL-17A的Th17细胞的比例显著升高,但是后面两个患者队列的Th17细胞总数没有增加。此外,在所有组中,重度GO患者的Th17.1细胞产生的IFN-γ最多,中重度GO患者的Th17.1细胞产生的IL-17A最多,重度和中重度GO患者的IL-17A和IFN-γ双重产生Th17.1细胞的比例显著增加。综上所述,重度GO、中重度GO和GD的效应T细胞免疫可能分别由Th17细胞或Th1细胞亚群所控制,并反映了Th17细胞系在GO发病进展过程中的实质功能可塑性。
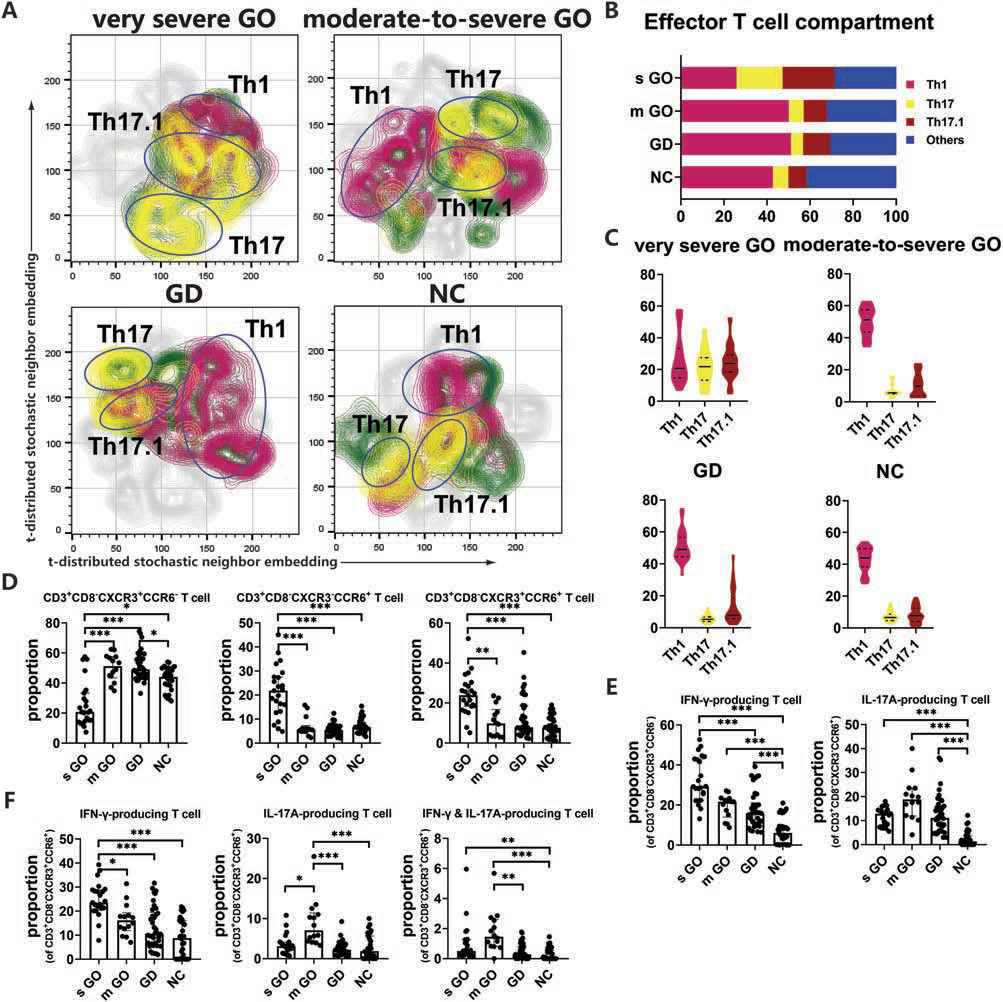
图1 重度GO和中重度GO患者及正常对照组效应T细胞的免疫表达
2、重度Graves眼病患者Th17.1细胞与血脂代谢的相关性研究
接下来研究者用UHPLC-QTOF-MS平台对重度GO患者进行脂质组学分析,在GC治疗前后共筛选和鉴定了79种不同的脂质物质。与治疗前相比,治疗后73种脂质代谢下调,6种上调。主要分为:PE、PC、FA、TAG、PI、HexCers等。使用ChemRICH分析显示,基于79种不同的脂质代谢产物,有9种脂质代谢途径发生了显著改变,其中TAG的幅度和趋势最为明显。此外,研究者还考察了治疗后GC敏感组和GC耐药组脂质代谢产物的差异,GC耐药患者血清中有11种物质上调。总的来说,GO患者Th17.1细胞周围脂质代谢的改变可能在GC治疗期间调节Th17.1细胞的功能和生存。
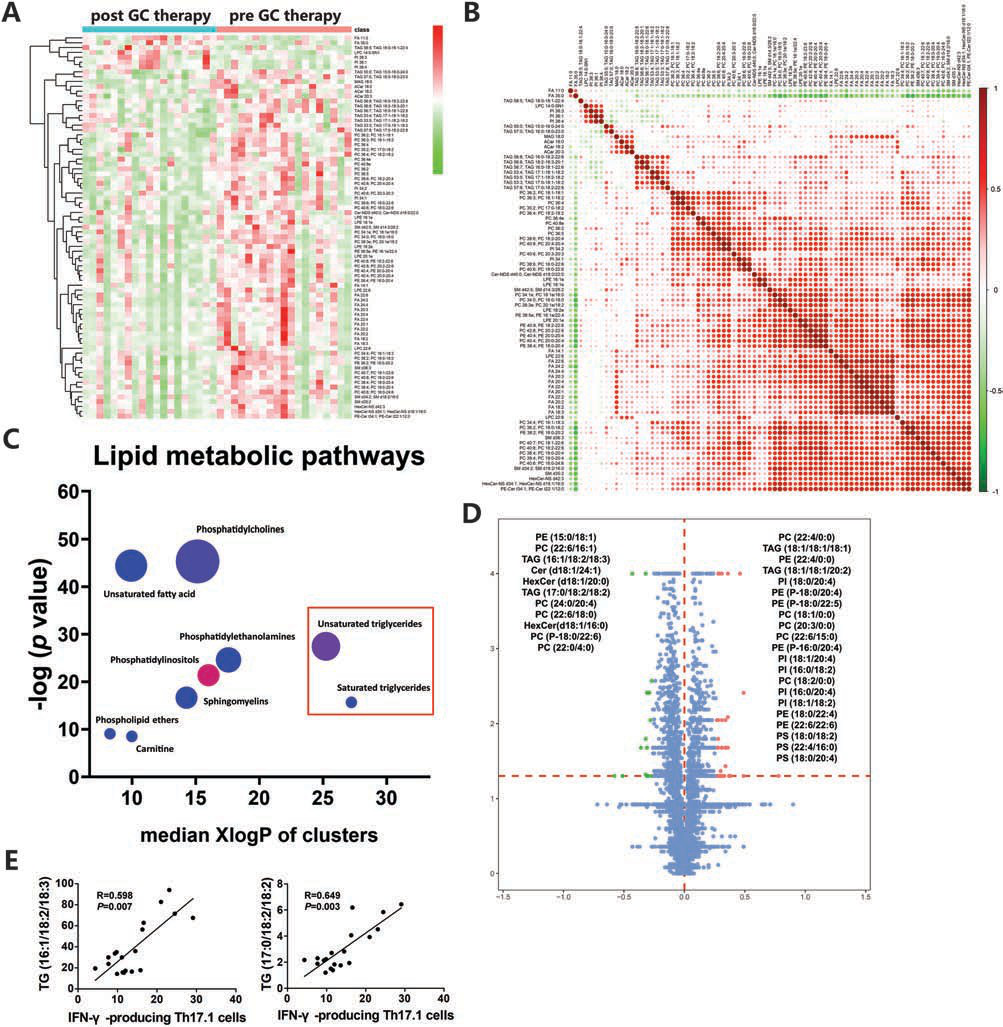
图2 糖皮质激素治疗Graves眼病(GO)患者的脂代谢异常
3、糖皮质激素抵抗、重度Graves眼病患者的球后组织以th17.1细胞免疫为主
最后,研究者进一步收集了6例手术后患者的GC抵抗、GO患者眼眶结缔组织,免疫组化结果显示,与GC敏感患者相比,GC抵抗患者的球后脂肪细胞纤维带或者血管周围存在IFN-γ+淋巴细胞浸润的现象,研究者还对GC耐药和敏感患者眼眶浸润细胞进行分类,WB显示GC耐药患者的Th17细胞表达了更多的转录因子Tbet和SATAT4,突出了Th17细胞转化成Th1的作用,GC敏感患者血清中的Th17表型保持稳定。GC耐药患者的眼眶提取物比GC敏感含有更高水平的TAG,血清中的水平也显著升高,而且在在培养抗GC患者血清中的Th17细胞中观察到Tbet和STAT4的表达增加,表现出Th1表型,与单独培养的Th17细胞相比,GC敏感患者血清中的Th17表型也保持稳定。
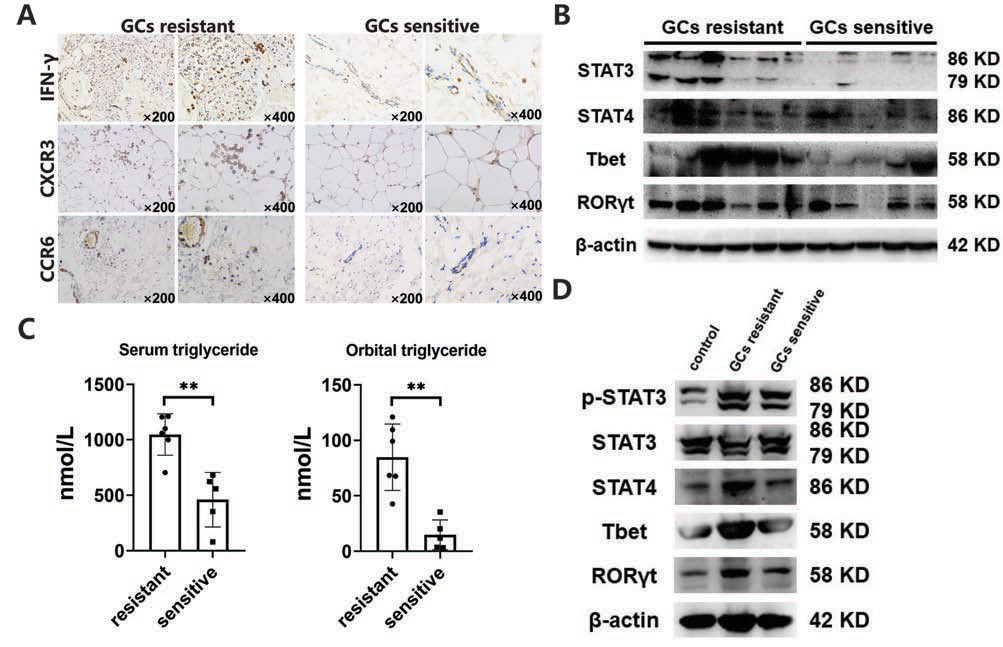
图3 AGs促进GO患者产生干扰素-γ的辅助性T细胞17.1(Th17.1)功能
综上所述,本文的研究首次为GD患者从Th1细胞免疫应答向Th17细胞免疫应答的转变过程提供了证据。更重要的是,研究者揭示了Th17.1细胞致病性与严重GO活动和发展之间的潜在相关性,并为了解Th17.1细胞功能与严重GO患者脂质代谢特征之间的关系奠定了基础。进一步研究了脂质代谢变化对GO中Th17.1细胞功能的影响,改善脂肪代谢和减轻严重GO患者Th17.1细胞炎症可能有助于降低GC或免疫抑制抵抗的程度。
FANG Sijie, ZHANG Shuo, HUANG Yazhuo, ZHOU Huifang*, FAN Xianqun*, et al. Evidence for associations between Th1/Th17 "Hybrid" phenotype and altered lipometabolism in very severe graves orbitopathy. Journal of Clinical endocrinology & Metabolism. 2020, 105(6): dgaa124.




